Конспект урока измерение скоростей молекул газа
Обновлено: 06.07.2024
Зная температуру, нетрудно вычислить среднюю кинетическую энергию молекул газа. После этого легко вычислить и среднюю скорость молекулы. А можно ли эту скорость измерить? Ведь молекулы так малы!
С помощью уравнения Е равно три вторых Ка Т можно найти средний квадрат скорости движения молекулы, подставив значение кинетической энергии в это уравнение.
Средняя кинетическая энергия молекул равна произведению массы молекулы эМ нулевое на среднюю скорость Вэ в квадрате деленное на 2.
В результате получим, что средний квадрат скорости Вэ в квадрате равно 3 умножить на Ка на Т и разделить на эМ нулевое.
Квадратный корень из этой величины называется средней квадратичной скоростью: средняя квадратичная скорость Вэ равна корню квадратному из дроби в числителе 3 КаТ, в знаменателе эМ нулевое.
Используя данную формулу, можно вычислить скорость молекул Например, скорость Вэ азота при t=0°С равна 500 метров в секунду.
Молекулы водорода при той же температуре имеют среднюю скорость Вэ равную 1800 метров в секунду.
Впервые были получены эти числа во второй половине XIX века, многие физики были удивлены, потому что скорости молекул газа по расчетам оказались больше, чем скорости артиллерийских снарядов! Это вызвало сомнения в справедливости кинетической теории.
Ведь вам известно, что запахи распространяются довольно медленно: нужно несколько десятков секунд, чтобы запах духов, пролитых в одном углу комнаты, распространился до другого угла. Это нетрудно объяснить. Из-за столкновения молекул траектория каждой молекулы представляет собой сложную ломаную линию, как вы видите на рисунке. Молекула развивает огромную скорость на прямолинейных отрезках ломаной, которая, как мы видим, очень часто меняет направление. Но если говорить о перемещении, а не о траектории, молекула проходит небольшой отрезок АВ, на рисунке он выделен синим цветом. Перемещение – это расстояние между начальной и конечной точкой пути, а траектория – это весь путь, который проходит молекула. Поэтому, если растянуть черную линию пройденного пути в одну прямую, то она окажется много больше расстояния AB.
Штерн в 1920 г. проводил эксперименты по определению скоростей молекул, с помощью которых подтвердил справедливость формул и найденных значений скорости. Для чего создал прибор Штерна состоящий из двух коаксиальных цилиндров A и B, жестко связанных друг с другом. Цилиндры, из которых откачан воздух, вращаются с постоянной угловой скоростью. Вдоль оси малого цилиндра натянута тонкая платиновая проволочка C, покрытая слоем серебра, по которой пропускают электрический ток. В стенке этого цилиндра имеется узкая щель O. Цилиндр B находится при комнатной температуре.
Вначале прибор неподвижен. При прохождении тока по нити слой серебра испаряется и внутренний цилиндр заполняется газом из атомов серебра. Некоторые атомы пролетают через щель O и, достигнув внутренней поверхности цилиндра B, осаждаются на ней. Поэтому прямо против щели образуется узкая полоска D серебра.
Затем цилиндры приводят во вращение с большим числом оборотов n в секунду (до 1500 1/c). Теперь за время t, необходимое атому для прохождения пути, равного разности радиусов цилиндров, цилиндры повернутся на некоторый угол φ (фи). В результате атомы, движущиеся с постоянной скоростью, попадают на внутреннюю поверхность большого цилиндра не прямо против щели O, а на некотором расстоянии s от конца радиуса, проходящего через середину щели: так как атомы движутся прямолинейно.
Если через Вэ в точке Бэ обозначить модуль скорости вращения точек поверхности внешнего цилиндра, то расстояние С равно произведению скорости вращения точек внешнего цилиндра на время Т или равно произведению 2 Пи на ЭН на радиус внешнего цилиндра эРвэ и на время т. Где произведение 2 πR (2Пи эР) – длина окружности внешнего цилиндра, а n количество оборотов.
Так как не все атомы серебра имеют одну и ту же скорость, расстояние s между участками на полосках D и D' (дэ штрих) с наибольшей концентрацией атомов серебра для различных атомов, будет различным. Следовательно, для этого расстояния можно определить среднюю скорость атомов, которая будет равна: отношению разности радиусов цилиндров ко времени т.
Сопоставив формулы по номерами 3 и 4, получим, что средняя скорость молекул равна 2 Пи ЭН умножить на разность радиусов внешнего и внутреннего цилиндров, разделить на расстояние s, умножить на радиус внешнего цилиндра эРвэ.
Зная концентрацию молекул, радиусы цилиндров и измерив среднее смещение полоски серебра, вызванное вращением прибора, можно найти среднюю скорость атомов серебра.
Определенные таким образом модули скоростей совпадают с теоретическим значением средней квадратичной скорости. Т.е. опыты Штерна являются экспериментальным доказательством справедливости формулы под номером 2, а, следовательно, и формулы под номером 1, согласно которой средняя кинетическая энергия молекулы прямо пропорциональна абсолютной температуре.
Средние скорости молекул превышают скорость звука и достигают сотен метров в секунду.
Рассмотрим пример решения задачи на определение средней квадратичной скорости.
Определите среднюю квадратичную скорость молекулы газа при 00С. Молярная масса газа М-0,019 кг/моль.
Запишем условие задачи.
Запишем формулу: средняя квадратичная скорость Вэ равна корню квадратному из дроби в числителе 3 КаТ, в знаменателе эМ нулевое.
Учтем то, что эм нулевое равно молярная масса разделить на число Авогадро и Т=273 К (кельвина), получим
средняя квадратичная скорость Вэ равна корню квадратному из дроби в числителе 3 КаЭНТ, в знаменателе эМ молярная масса, подставим значение величин и вычислим: средняя квадратичная скорость молекулы газа при 0 градусов Цельсия равна 600 метров в секунду.
Цель данной разработки- описать методику проблемного обучения на основе изучения новой темы "Определение скоростей молекул газа".
Методика использования сводится к следующему: педагог ставит перед учащимся проблему, это можно сделать с помощью вопросов
или системы направляющих вопросов, которые вызывают интеллектуальное затруднение, направляют мыслительную деятельность на решение проблемы.
| Вложение | Размер |
|---|---|
| Разработка урока на основе проблемного обучения | 79.5 КБ |
Предварительный просмотр:
Агентство по управлению имуществом Пермского края
Государственное образовательное учреждение среднего профессионального
Урока по физике на тему:
Зверева Ольга Владимировна преподаватель физики.
Традиционное обучение, как правило, обеспечивает учащихся системой знаний и развивает память, но мало направлено на развитие мышления, навыков самостоятельной деятельности. Проблемное обучение устраняет эти недостатки, оно активизирует мыслительную деятельность учащихся, формирует познавательный интерес.
Проблемное обучение, основанное на закономерностях развития мышления, призвано научить учеников самостоятельно мыслить, самостоятельно получать знания, анализировать и делать выводы. При проблемном подходе к обучению есть возможность уйти от механического запоминания. Когда перед учащимися ставится учебная проблема, создается тем или иным способом проблемная ситуация, у них появляется интерес, они активно включаются в процесс решения проблемы - все это способствует лучшему усвоению материала, причем большая часть усваивается непроизвольно. Ученик учится мыслить научно.
Занятия, основанные на проблемном обучении должны занимать заметное место в преподавании физики, так как они повышают интерес учащихся к предмету, заставляют их работать разнообразнее, интенсивнее, с выдумкой и, конечно, поднимают авторитет учителя.
Несомненно, с помощью таких занятий реализуется одна из функций учителя- создание положительного, эмоционального отношения к знаниям.
Такие занятия требуют от учителя знаний, умений, тщательной подготовки, но приносят удовлетворения в работе, дают возможность установить деловые и теплые отношения с учащимся.
- Описать организацию учебного процесса, выстроенного с применением проблемного обучения на уроках физики;
- Описать методику введения проблемного обучения на уроках физики;
Методика использования сводится к следующему: педагог ставит перед учащимся проблему, это можно сделать с помощью вопросов или системы направляющих вопросов, которые вызывают интеллектуальное затруднение, направляют на мыслительную деятельность на решение проблемы.
Для результативности применяемой методики можно провести диагностику, результаты которой показывают на сколько данная методика применима к учащимся.
2. Образовательные задачи занятия:
- усвоение новых знаний:
1. Научных фактов:
- несовместимость больших значений скоростей молекул газа, полученных теоретически;
- основная часть молекул движутся со средней скоростью;
- распределение по скоростям носит характер статистической закономерности;
- распределение молекул по скоростям зависит от температуры газа;
- в пучке присутствуют молекулы с разными скоростями.
2. Эмпирических понятий:
- скорость свободного пробега молекул;
- распределение молекул по скоростям (распределение Максвелла);
3. Эмпирических законов:
- формирование новых умений:
- обобщать данные опытов, выявлять эмпирические закономерности в протекании физических явлений;
- читать рисунки, схемы, таблицы;
- умение применять математические знания на уроках физики;
- умение выполнять научно- технические исследования;
3. Дидактическая структура занятия:
Цель: изучение нового материала в форме поискового физического эксперимента.
1. Организационный этап
Контроль учителем готовности класса к уроку
2. Вступительное слово
Формулировка учебной задачи, плана занятия.
3. Изучение нового материала
Рассмотрение и изложение материала в форме поискового физического эксперимента по обобщенному плану:
Сформулировать (уяснить) проблему исследования.
Выдвинуть и обосновать гипотезу.
Определить согласно гипотезе цель эксперимента.
Разработать проект установки.
Определить состав оборудования и собрать экспериментальную установку.
Определить порядок деятельности.
Определить рациональный способ записи.
Реализовать порядок деятельности.
Реализовать порядок записи.
Проанализировать результаты, сформулировать вывод.
Создание проблемных ситуаций;
Система направляющих вопросов;
Демонстрация модели прибора Штерна
4. Домашнее задание
4. Демонстрационный эксперимент:
Цель: демонстрация способа определения скорости движения молекул газа в опыте Штерна.
Оборудование: 1) вращающийся диск с принадлежностями;
2) метр демонстрационный;
6) шарик стальной;
В диске, установленный по уровню, закрепляют трубку с желобом для пуска шарика так, чтобы конец желобка совпал с осью вращения диска. На диске укрепляют барьер-ловушку.
Пускают из центра диска шарик и замечают место, куда он попадает на барьере.
Приводят диск в равномерное движение с определенным числом оборотов в секунду, которое отмечают по тахометру и снова пускают шарик. Измеряют радиус диска и расстояние, на которое сместился шарик в этом опыте.
Литература для учителя:
Г. Я. Мякишев, Б. Б. Буховцев Физика 10; Л.Ландау, Китайгородский т.1 Молекула; Н.М.Шахмаев Элементарный курс физики; О.Ф.Кабардин, С.И. Кабардина Задания для итогового контроля знаний учащихся по физике; Н. М. Шахмаев Молекулярная физика.
Кинетическая теория идеального газа основана на том, что газ состоит из беспорядочно движущихся частиц- молекул. Но с какой скоростью они движутся? На последних занятиях мы с вами неоднократно получали формулу для вычисления средней квадратичной скорости молекул. Для примера средняя квадратичная скорость молекул водорода при 20 градусах равна примерно 1000 м/с. (вычисления сделать вместе с учениками). Для сравнения привести примеры: скорость движения молекул азота при 0 градусах – 500 м/с, максимальная скорость автомобиля – 500 м/с, максимальная скорость пассажирского самолета – 700 м/с, скорость движения Луны вокруг Земли – 1000 м/с.
А теперь поставите себя на место ученых 19 века, когда были получены эти данные, возникли сомнения в правильности самой кинетической теории. Ведь известно, что запахи распространяются довольно медленно: нужно время порядка десятков секунд, чтобы запах духов, пролитых в одном углу комнаты, распространяются до другого угла.
Поэтому возникает вопрос: какова на самом деле скорость молекул?
Это и будет цель нашего урока, эта проблема, которую необходимо разрешить.
Какую скорость находить и измерять? Когда запах духов распространяется, мешает ли что-то молекулам духов? (мешают молекулы воздуха). Как это влияет на скорость направленного движения молекул? (Она уменьшается). Теперь в задаче мы получили большую скорость, и ничего не мешает двигаться ей. Тогда это скорость какая? Чего? ( Скорость свободного пробега молекул). А как же её измерить, определить её значение на практике? Давайте решим эту задачу, пишем: пусть имеется 1 молекула. Нужно определить скорость свободного пробега молекул. Как движутся молекулы между столкновениями? (равномерно). Пусть молекула проходит 1 метр, время найдем при скорости водорода 1930 м/с, получилось 0,00052 с. Как видно время очень маленькое, как же его измерить? Возникает опять проблема!
Что бы ответить на эти вопросы, рассмотрим пример: пусть летит утка со скоростью на высоте, и в момент выстрела находилась на каком – то расстоянии. Нужно ли ждать охотнику пока утка подлетит и будет прямо над ним? ( Нет, потому что нужно время для полета пули). Охотник выстрелил вертикально и попал в неё. Найти скорость пули!
Каким образом решение этой задачи можно использовать для измерения скорости молекул? (Проведем аналогию: пуля – молекула, утка – мишень, находящаяся на известном расстоянии). Скорость молекул находится как скорость мишени*расстояние, которое пролетает молекула и разделить на расстояние в момент выстрела (Vмол=(V мишени * R)/ S) (1). Неизвестна скорость мишени. Как заставить её двигаться? Линейные перемещения использовать не очень хорошо ( не удобно). Лучше использовать вращательные движения мишени. А если мишень совершает вращательные движения, то вспомним связь угловой скоростью с линейной V=w*R. Будем считать, что R=h тогда формула (1) перепишется
V мол =(2pi*n*R 2 )/S (3)
Цель исследования - измерить, подсчитать скорость молекул по известной формуле.
Мы с вами пришли к тому, что мишень должна вращаться, давайте отойдем от понятия мишени. Если что-то вращается, то какой формы это должно быть? (Круглой, в форме цилиндра). Будем считать, что мишень находится внутри цилиндра. Теперь вспомним, что мы вели речь лишь об одной молекуле. Может ли она оставить след? (нужно взять много молекул). Скорости молекул разные по величине и по направлению, четкого следа не получим. Тогда как сделать так, чтобы скорости по направлению были одинаковыми? (выделим узкий пучок с помощью диафрагмы). Теперь вопрос: откуда взять эти молекулы? (Расплавить металл в печи, под действием электрического тока верхний слой испаряется и цилиндр заполняется газом).
Как обеспечить, чтобы молекулы при движении в цилиндре не сталкивались? (Откачать воздух, создать вакуум).
Да, давайте подведем некий итог: мы изобрели сами прибор, с помощью которого мы сможем измерить скорость молекул.
Чем наша установка нехороша? (Громоздкая). Да, и нужно непрерывно с помощью работающего насоса поддерживать вакуум. Как сделать компактнее установку? Можем все три детали установки соединить в одну? ( Печь перенести в цилиндр). Лучше взять пластинку или проволочку, которая нагревается. Теперь наша установка приобретает вид:
Где создать вакуум? И что в нашей установке будет играть роль диафрагмы? (Удобно использовать 2 цилиндра, вложенных в друг друга. В одном цилиндре будет щель, которая играет роль диафрагмы). Теперь установка имеет вид:
платиновая нить, покрытая тонким слоем серебра, располагается вдоль оси внутри цилиндра;
пространство внутри цилиндра 2 откачивают насосом до давления 10 -5 -10 -6 мм рт ст. при пропускании электрического тока через проволоку она разогревалась до температуры выше температуры плавления серебра 961,9 0 С. Стенки внешнего цилиндра охлаждались, чтобы молекулы серебра лучше оседали на пути экрана.
установку приводили во вращение с угловой скоростью 2500 – 2700 об/мин. Значения скоростей получались близкой к скорости, вычисленной по формуле (3) , что находится в согласии с молекулярно- кинетической теорией.
6. Порядок деятельности:
Включить ток, создать испарение и получить след молекул при неподвижной установке.
Включить установку и измерить частоту.
Получить след молекул при подвижной установке.
Вычислить скорость по формуле (3)
7, 8,9: Показ способа определения скорости движения молекул газа в опыте Штерна
Результаты опыта Штерна:
Цилиндр подвижен: против щели образуется узкая полоска серебра одинаковой толщины.
Цилиндр вращается, полоска серебра смещается.
Подставляя данные в формулу (3) Штерн получил следующие значения скоростей при 0 0 С (водород-1838 м/с, азот- 493 м/с, кислород- 401 м/с)
Из формулы (3) следует, что положение полоски молекул зависит от скорости молекул.
В разрезе след серебра имел такую форму, что в пучке присутствуют молекулы с разными скоростями (распределения Максвелла).

Этот урок посвящен изучению того, каким способом можно измерить скорость молекул газа. Мы рассмотрим один из самых известных экспериментов в этой области – опыт Штерна.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Измерение скоростей молекул газа"
На прошлых уроках мы вывели уравнение, позволяющее связать среднюю кинетическую энергию молекул и температуру.
Как вы знаете, средняя кинетическая энергия молекул равна половине произведения массы молекулы и среднего значения квадрата скорости молекул:

Таким образом, зная температуру газа, мы можем найти среднее значение квадрата скорости его молекул:

Расчеты говорят о том, что при 0 о С, средняя скорость молекул азота достигает 500 м/с, а средняя скорость молекул водорода — 1800 м/с. Во второй половине 19 века это привело некоторых физиков в замешательство. Ведь всем хорошо известно, что запахи распространяются сравнительно медленно. Как же тогда получается, что молекулы газа двигаются с огромными скоростями, а само облако газа двигается в сотни раз медленнее?
Ответ на этот вопрос достаточно простой: молекулы двигаются беспорядочно, а потому их перемещения в сотни раз меньше пройденного пути. В качестве аналогии мы опять можем привести футбол. За один матч футболисты пробегают более десяти километров, однако, все это время они остаются в пределах футбольного поля, размеры которого равны 120 х 60 м.
Кроме расчетов скоростей молекул газа с помощью теории, существуют экспериментальные методы измерения скоростей. На сегодняшнем уроке, мы рассмотрим опыт Штерна, проведенный в 1920 году. Этот опыт был одним из первых экспериментальных подтверждений состоятельности молекулярно-кинетической теории.

Прибор Штерна представляет собой два коаксиальных цилиндра (то есть эти цилиндры обладают общей осью симметрии).
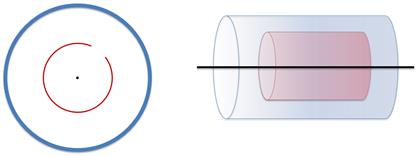
Из цилиндров откачан весь воздух. Вдоль оси малого цилиндра натянута тонкая платиновая проволока, покрытая серебром, а также в малом цилиндре имеется небольшая щель.
По проволочке пропускают электрический ток, с целью заставить серебро испаряться. В результате испарения, малый цилиндр заполняется газом из атомов серебра.
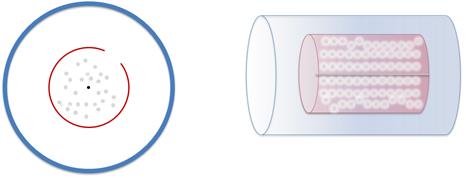
Разумеется, часть этих атомов пролетают через щель и оседают на внутренней стенке большого цилиндра. Этот слой серебра имеет определенное положение — прямо напротив щели в малом цилиндре.
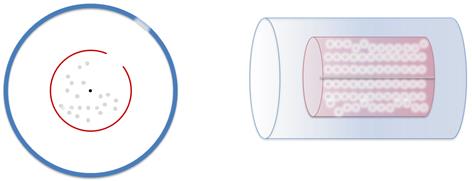
После этого, цилиндры приводят во вращение с одинаковой угловой скоростью и большой частотой (около 1500 об/с). Теперь атомы будут осаждаться не прямо напротив щели, поскольку за то время, пока они проходят расстояние от стенки малого цилиндра до стенки большого цилиндра, цилиндры поворачиваются на некоторый угол. Более того, слой серебра будет немного размытый из-за того, что не все атомы серебра двигаются с одинаковыми скоростями.
Обозначим за R радиус большого цилиндра, а радиус малого цилиндра — за r. Обозначим за d расстояние от конца радиуса, проходящего через центр щели до наибольшей концентрации атомов серебра после начала вращения. (Дело в том, что не все атомы имеют одинаковую скорость, поэтому, не все они попадают в одну и ту же точку). Поэтому, расстоянию d будет соответствовать средняя скорость атомов серебра:

Запишем теперь, что расстояние d равно:

Изучая криволинейное движение, мы убедились, что скорость вращения можно выразить через радиус вращения и частоту:

Из полученного выражения выразим время:

А теперь, это время подставим в формулу для средней скорости:

Таким образом, получили выражение, в котором средняя скорость задана через радиусы цилиндров, частоту вращения и расстояние d. Конечно же, радиусы цилиндров и расстояние d можно измерить. Частоту вращения задает сам экспериментатор, поэтому, она тоже известна. Модули скоростей, измеренные подобным способом, совпадают с теоретическим значением в пределах экспериментальной ошибки. Это говорит о том, что теоретическая формула, по которой мы вычисляли скорость, оказалась верна. Следовательно, верно и уравнение, связывающее среднюю кинетическую энергию молекул и температуру тела по абсолютной шкале Кельвина:
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Методическая разработка учебного занятия по теме:
Определение скоростей молекул газа
Профессия: 23.01.03 Автомеханик
Дисциплина: ОДП.03 Физика
Преподаватель: Зверева Ольга Владимировна
Пояснительная записка
План занятия
Тема учебного занятия: Определение скоростей молекул газа
Ввести новые понятия: средняя скорость, средняя квадратичная скорость, наиболее вероятная скорость, распределение скоростей молекул газа
Вывести формулу для средней квадратичной скорости
Определить среднюю квадратичную скорость молекул газа, наиболее вероятную скорость
-развивающая
Способствовать развитию умения анализировать, предполагать, выдвигать гипотезы, наблюдать и делать выводы
Способствовать развитию умения грамотно выражать свои мысли.
Содействовать развитию элементов общих компетенций
-воспитательная
Мотивировать на активную деятельность обучающихся на уроке.
Мотивировать на познавательный интерес к предмету и окружающим явлениям
Тип учебного занятия: урок изучения нового материала
Используемые технологии: элементы проблемно-диалогического обучения, элементы информационных технологий.
Формируемые общие компетенции, определенные стандартом ФГОС:
ОК 1. Понимать сущность и социальную значимость своей будущей профессии, проявлять к ней устойчивый интерес.
ОК 2. Организовывать собственную деятельность, исходя из цели и способов ее достижения, определенных руководителем.
ОК 3. Анализировать рабочую ситуацию, осуществлять текущий и итоговый контроль, оценку и коррекцию собственной деятельности, нести ответственность за результаты своей работы.
ОК 6. Работать в команде, эффективно общаться с коллегами, руководством, клиентами
Используемые методы обучения:
наглядный: демонстрация презентации, виртуальный эксперимент
практический: работа с вычислениями.
Используемые формы организации познавательной деятельности студентов: коллективная и индивидуальная
Учебно-методическое обеспечение урока:
- технические средства: компьютер, проектор, проекционный экран.
Межпредметные связи: математика.
Предполагаемые результаты:
Обучающиеся должны знать: строение газов, положения МКТ, среднюю квадратичную скорость движения молекул, наиболее вероятную скорость молекул, распределение Максвелла по скоростям, зависимость скорости молекул от температуры и массы одной молекулы газа.
Обучающиеся должны уметь:
Находить среднюю квадратичную скорость движения молекул.
Структура занятия:
Название этапа
Деятельность педагога
Деятельность обучающихся
Приветствие. Демонстрирует анимированные картинки на слайде 1. Вопрос: что общего вы видите на демонстрации?
Подводящие к теме вопросы: Как движутся молекулы? Можно ли вычислить скорость молекул? Чему равна эта скорость?
Предлагает предположить методы определения скоростей молекул – создает условия для формулирования цели занятия.
Предлагает оценить настроение в начале занятия.
Высказывают собственные мысли.
Настраиваются на предстоящую работу.
Выдвигают варианты формулировок цели, участвуют в их обсуждении. Анализируют.
Поднимают листы со смайлами.
Актуализация опорных знаний
Организация фронтального опроса ключевых понятий: положения МКТ, свойства газа, от чего зависит скорость молекул, одинаковы ли скорости молекул в сосудах. (слайд 3-4)
Отвечают на вопросы, сравнивают, анализируют
Записывают в рабочие листы ответ
Первичное усвоение материала
Объясняет с помощью демонстрационного слайда 5 новые понятия: средняя скорость, средняя квадратичная скорость, вывод формулы.
Предлагает решить задачу №1: вычислить скорость молекул водорода при температуре 20 0 теоретически. Образец пишет на доске.
Мотивирующий прием: сравнивает вычисленную скорость со скоростью реальных объектов. Возникает проблема, противоречие теоретического ответа и жизненного опыта. Ведет подводящий диалог от проблемы, методы поиска решения к задаче № 2: измерение скоростей молекул газа на опыте.
Организует работу обучающихся с ЭОР (приложение)
Заполняют рабочие листы
Решают в рабочих листах, работают под руководством педагога. Анализируют полученные ответы, сравнивают с жизненным опытом.
Просмотр, наблюдение, выдвигают гипотезы, предполагают, делают выводы. Заполняют рабочие листы.
Первичное закрепление материала
Ведет диалог, демонстрирует вопросы и качественные задания (слайд 7-8):
Средние скорости молекул превышают скорость звука и достигают сотен м/с. Почему же запах духов в комнате из одного угла в другой распространяется довольно медленно порядка десятка секунд?
Как изменится средняя квадратичная скорость движения молекул при увеличении температуры в 4 раза?
Какие молекулы в атмосфере движутся быстрее: молекулы азота или молекулы кислорода?
При сгорании бензинового и дизельного топлива образуются выхлопные газы. На выходе t газов бензинового двигателя – 400 0 C , а дизельного – 200 0 С.
-От какого двигателя запах выхлопных газов дойдет быстрее до наблюдателя?
-Определите, во сколько раз средняя квадратичная скорость молекул выхлопного газа бензинового двигателя будет больше, чем дизельного? За основу взять СО 2 .
опишите скорость молекул по схеме: существительное –2 прилагательных, раскрывающих тему—3 глагола, описывающих действия—фраза, состоящая из нескольких слов, выражающая суть или отношение к теме—слово-резюме

Бесплатное участие. Свидетельство СМИ сразу.
До 500 000 руб. ежемесячно и 10 документов.
Данный материал представлен в формате Word и разработан в помощь учителю при проведении урока в курсе физики 10 класса по соответствующей теме. Это краткий конспект урока, помогающий распределить время и этапы урока. Можно использовать как рабочий лист этап "опрос", распечатав его для учащихся. Материал полностью готов к распечатке
Цель: ____________________________________________________________________________________________ _________________________________________________________________________________________________ Измерение скоростей молекул газа. § 69 ОПРОС 1.Перечислите основные макроскопические параметры __________________________________________________ 2.Как без термометра определить степень нагретости тела?_______________________________________________ _________________________________________________________________________________________________ 3.Для чего используют термометр? ___________________________________________________________________ 4.Какие виды термометров вы знаете? ________________________________________________________________ _________________________________________________________________________________________________ 5. На чём основан принцип действия термометра? ______________________________________________________ _________________________________________________________________________________________________ 6.Как правильно измерять температуру тел? ___________________________________________________________ _________________________________________________________________________________________________ 7.Что такое тепловое равновесие? ____________________________________________________________________ _________________________________________________________________________________________________ 8.Что температура? ____________________________________________________________________ _________________________________________________________________________________________________ 9.Приведите примеры установления теплового равновесия тел, окружающих нас в повседневной жизни. _________________________________________________________________________________________________ _________________________________________________________________________________________________ _________________________________________________________________________________________________ 10.Что можно сказать о средних Ек молекул газов при тепловом равновесии? _______________________________ _________________________________________________________________________________________________ 11.Что называют абсолютным нулём температуры? ____________________________________________________ _________________________________________________________________________________________________ 12.Какова связь шкалы Цельсия и Кельвина? __________________________________________________________ _________________________________________________________________________________________________ характеризует Зная Т, нетрудно вычислить Ēк молекул, а затем и среднюю молекулы. НОВАЯ ТЕМА υ , где , тогда Средняя квадратичная скорость υ≈ 500 м/с 1800 м/с При t=00С: молекулы азота имеет υ≈ молекулы водорода Учёные были ошеломлены. Высказывались сомнения в справедливости теории. Известно, что запахи распространяются довольно медленно. Объяснение: Изза столкновения молекул траектория каждой – это запутанная ломаная линия. Большие скорости молекула имеет на прямолинейных отрезках ломанной. Путь АВ
Читайте также:

