Конспект мкт агрегатные состояния вещества
Обновлено: 07.07.2024
Раздел ОГЭ по физике: 2.1. Молекула – мельчайшая частица вещества. Агрегатные состояния вещества. Модели строения газов, жидкостей, твердых тел.
Основы молекулярно-кинетической теории
Существует множество явлений природы, которые можно понять, лишь зная строение вещества. К таким явлениям относятся, например, процессы нагревания и охлаждения тел, превращения вещества из твёрдого состояния в жидкое и газообразное, образования тумана и др.
- Все вещества состоят из мельчайших частиц – молекул и атомов. Молекулы разделены промежутками.
- Молекулы находятся в беспрерывном хаотическом движении.
- Между молекулами существуют силы взаимодействия (притяжение и отталкивание).
Атом – наименьшая частица химического элемента, которая является носителем его химических свойств. Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов, движущихся по законам квантовой механики. Размеры атома ~ 10 –10 м.
Молекула – наименьшая устойчивая частица вещества, обладающая всеми его химическими свойствами и состоящая из одинаковых (простое вещество) или разных (сложное вещество) атомов, объединённых химическими связями. При уменьшении расстояния между молекулами сила притяжения увеличивается медленнее, чем сила отталкивания.
Доказательством положения 1 МКТ служат факты, установленные в ходе наблюдений и экспериментов. К таким фактам относятся сжимаемость тел, растворимость веществ в воде и др. Так, если растворить немного краски в воде, то вода окрасится. Если каплю этой воды поместить в другой стакан с чистой водой, то эта вода также окрасится, только цвет её будет менее насыщенным. Можно повторить эту операцию ещё несколько раз. В каждом случае раствор будет окрашен, только более слабо, чем в предыдущем. Это значит, что капля краски делится на частицы. Приведённые факты и описанный опыт позволяют сделать вывод о том, что тела не сплошные, они состоят из маленьких частиц.
О том, что тела не сплошные, а между частицами, из которых они состоят, существуют промежутки, свидетельствует то, что газ в цилиндре можно сжать поршнем, можно сжать воздух в воздушном шаре, ластик или кусок резины, тела сжимаются при охлаждении и расширяются при нагревании. Так, ненагретый шарик свободно проходит через кольцо, диаметр которого чуть больше диаметра шарика. Если шарик нагреть в пламени спиртовки, то он в кольцо не пройдет.
Из опытов, которые были рассмотрены выше, следует, что вещество можно разделить на отдельные частицы, сохраняющие его свойства. Однако существует определённый предел деления вещества, т.е. существует самая маленькая частица вещества, которая сохраняет его свойства. Меньшей частицы, которая сохраняет свойства данного вещества, просто не существует. Наименьшая частица вещества, которая сохраняет его химические свойства, называется молекулой.
Опыты, которые были описаны, говорят о том, что молекулы имеют маленькие размеры. Увидеть их невооруженным глазом невозможно. Диаметр крупных молекул примерно 10 –8 см. Поскольку молекулы так малы, то в телах их содержится очень много. Так, в 1 см 3 воздуха содержится 27*10 18 молекул.
Масса молекул, так же как и её размеры, очень мала. Например, масса одной молекулы водорода равна 3,3 * 10 –24 г или 3,3 * 10 –27 кг. Масса молекул одного и того же вещества одинакова. В настоящее время масса и размеры молекул различных веществ определены достаточно точно.
Молекулы состоят из ещё более мелких частиц, которые называются атомами. Например, молекулу воды можно разделить на водород и кислород. Однако водород и кислород уже другие вещества, и они обладают свойствами, отличными от свойств воды. Разложить молекулу воды на такие вещества можно в процессе химической реакции.
Молекула воды состоит из двух атомов водорода и одного атома кислорода; молекула поваренной соли — из одного атома натрия и одного атома хлора. Молекула сахара более сложная: она состоит из б атомов углерода, 12 атомов водорода и 6 атомов кислорода, а молекула белков состоит из тысячи атомов.
Существуют вещества, молекулы которых содержат однородные атомы. Например, молекула водорода состоит из двух атомов водорода, молекула кислорода — из двух атомов кислорода.
В природе есть вещества, которые состоят не из молекул, а из атомов. Их называют простыми. Примерами таких веществ могут служить алюминий, железо, ртуть, олово и др.
Любое вещество, независимо от того, как оно получено, содержит одни и те же атомы. Например, молекула воды, полученная при таянии льда, или из сока ягод, или налитая из-под крана, содержит два атома водорода и один атом кислорода. Молекула кислорода, извлечённая из атмосферного воздуха или полученная в ходе какой-либо химической реакции, содержит два атома кислорода.
- Положение 2 МКТ. Молекулы находятся в непрерывном беспорядочном (хаотическом) движении. Поскольку молекулы малы, то непосредственно наблюдать и доказать их движение невозможно. Однако целый ряд экспериментальных фактов и наблюдаемых явлений является следствием движения молекул. К ним относятся прежде всего броуновское движение и диффузия.
- Положение 3 МКТ. Молекулы взаимодействуют между собой, между ними действуют силы и притяжения и отталкивания.
Наблюдения показывают, что тела не распадаются на отдельные молекулы. Твёрдые тела, например деревянную палку, металлический стержень, трудно растянуть или сломать. Их также трудно и сжать. Нелегко сжать и жидкость в сосуде. Газы сжать легче, но всё равно нужно приложить для этого некоторое усилие.
Если тела не распадаются на молекулы, то очевидно, что молекулы притягиваются друг к другу. Взаимное притяжение удерживает молекулы друг около друга.
До того, как цилиндры зачистили, они разъединялись, поскольку поверхности цилиндров имели неровности, которые были устранены при зачистке. Поверхности стали гладкими, и это привело к уменьшению расстояний между молекулами, находящимися на поверхностях цилиндров, когда их прижали друг к другу. Следовательно, силы притяжения между молекулами действуют на малых расстояниях. Эти расстояния равны примерно размерам молекулы. Именно поэтому нельзя разбив чашку и соединив осколки, получить целую чашку. Нельзя, разломив палку на две части и соединив их, получить целую палку.
Наряду с силами притяжения, между молекулами действуют силы отталкивания, которые препятствуют сближению молекул. Это объясняет то, что тела трудно сжать, сжатая пружина принимает первоначальную форму после прекращения действия на неё внешней силы. Это происходит потому, что при сжатии молекулы сближаются и силы отталкивания, действующие между ними, возрастают. Они и приводят пружину в первоначальное состояние.
При растяжении тела сила отталкивания уменьшается в большей степени, чем сила притяжения. При сжатии тела сила отталкивания увеличивается в большей степени, чем сила притяжения.
Три агрегатных состояния
Вещества могут находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном. Свойства тел в разных агрегатных состояниях различны.
Так, твёрдое тело имеет определённую форму и определённый объём. Его трудно сжать или растянуть; если его сжать, а потом отпустить, то оно, как правило, восстанавливает свою форму и объём. Исключение составляют некоторые вещества, твёрдое состояние которых близко по своим свойствам к жидкостям (пластилин, воск, вар).
Жидкость принимает форму сосуда, в который она налита. Это говорит о том, что жидкость в условиях Земли не имеет своей формы. Только очень маленькие капли жидкости имеют свою форму — форму шара.
Объём жидкости изменить чрезвычайно трудно. Так, если набрать воду в насос, закрыть отверстие внизу и попытаться сжать воду, вряд ли это удастся. Это означает, что жидкость имеет собственный объём.
В отличие от жидкости объём газа изменить довольно легко. Это можно сделать, сжав руками мяч или воздушный шарик. Газ не имеет собственного объёма, он занимает полностью объём сосуда, в котором находится. То же можно сказать и о форме газа.
Таким образом, твёрдые тела имеют собственные форму и объём, жидкости имеют собственный объём, но не имеют собственной формы, газы не имеют ни собственного объёма, ни собственной формы. Твёрдые тела и жидкости трудно сжать, газы легко сжимаемы.
Объяснить эти свойства тел можно, используя знания о строении вещества.
Поскольку газы занимают весь предоставленный им объём, то очевидно, что силы притяжения между молекулами газа малы. А это значит, что молекулы находятся на сравнительно больших расстояниях друг от друга. В среднем они в десятки раз больше расстояний между молекулами жидкости. Это подтверждается тем, что газы легко сжимаемы.
Малые силы притяжения влияют и на характер движения молекул газа. Молекула газа движется прямолинейно до столкновения с другой молекулой, в результате чего меняет направление своего движения и движется прямолинейно до следующего столкновения.
Твёрдые тела трудно сжать. Это связано с тем, что молекулы находятся близко друг от друга и при небольшом изменении расстояния между ними резко возрастают силы отталкивания. Сравнительно большое притяжение между молекулами твёрдых тел приводит к тому, что они сохраняют форму и объём.
Атомы или молекулы большинства твёрдых тел расположены в определённом порядке и образуют кристаллическую решётку. На рисунке 63 изображена кристаллическая решётка поваренной соли. В узлах кристаллической решётки находятся атомы натрия (Na) и хлора (Сl). Частицы твёрдого тела (атомы или молекулы) совершают колебательное движение относительно узла кристаллической решётки.
В жидкостях молекулы расположены также довольно близко друг к другу. Поэтому их трудно сжать, и они имеют свой объём. Однако силы притяжения между молекулами жидкости не настолько велики, чтобы жидкость сохраняла свою форму.
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Государственное бюджетное общеобразовательное учреждение
Краснодарского края школа-интернат спортивного профиля.
Урок- исследования
Учитель физики:
Волошина О.А.
Фамилия, имя, отчество учителя: Волошина Ольга Андреевна
Название УМК: Физика 7 класс: учебник для общеобразовательных учреждений/ А.В. Перышкин. - 16-е издание, доп.- М.: Дрофа, 2012
Предмет: физика
Тема урока : Различные состояния вещества и их объяснение на основе молекулярно-кинетических представлений.
Тип урока : комбинированный.
Цель урока : образовательная : изучить сходство и различие агрегатных состояний вещества с позиции МКТ, рассмотреть агрегатные состояния вещества на примере воды
развивающая: развитие логического и образного мышления
воспитательная: воспитание исследовательских свойств .
Планируемые результаты:
личностные:
формирование ответственного отношения к учению на основе мотивации к обучению и познанию;
формирование осознанного, уважительного и доброжелательного отношения к другому человеку, его мнению;
формирование коммуникативной компетентности в общении и сотрудничестве со сверстниками и взрослыми в процессе учебной деятельности.
метапредметные :
умение определять понятия, создавать обобщения, классифицировать, строить рассуждение, умозаключение и делать выводы;
умение создавать, применять различные продукты для решения учебной задачи;
умение оценивать правильность выполнения учебной задачи, собственные возможности её решения;
предметные :
знать: основные положения МКТ; основные свойства трёх состояний вещества
уметь: решать задачи на применение данной темы.
Рекомендуемые образовательные ресурсы.
I . Организационный момент (мотивация к учебной деятельности)
Цель этапа: включение обучающихся в деятельность на личностно-значимом уровне
Здравствуйте. Садитесь. Проверьте, все ли готовы к уроку? У вас должны быть на парте учебник, тетрадь, ручки, карандаши и дневник.
Итак, начнем сегодняшний урок.
Проверяют свою готовность к уроку.
Планирование учебного сотрудничества с учителем и сверстниками (К).
II . Актуализация знаний
Учитель задает вопрос :
- Из чего состоит тело?
-А из чего состоит вещество?
-Какие явления показывают, что вещества состоят из частиц, разделенных промежутками?
-Как показать, что эти частицы малы?
- Как доказать, что эти частички непрерывно движутся?
Ученики отвечают на вопрос учителя.
Ученики высказывают свое мнение, вспоминая ранее изученный материал.
Умение выражать мысли (К).
Построение логической цепи (П).
Постановка цели урока
Вода – наиболее распространённое в природе вещество. Водяной пар – газообразное состояние воды. Жидкая вода –жидкое её состояние. Лёд – твёрдое состояние воды.
Как называется тема сегодняшнего урока?
Какова главная цель урока?
Ученики внимательно слушают и отвечают на вопрос учителя:
Учащиеся формулируют цель: изучить сходство и различие агрегатных состояний вещества.
Умение выражать мысли (К).
Планирование, целеполагание (Р).
Самостоятельное выделение и формулирование познавательной цели (П).
III . Проблемное объяснение нового материала
Цель этапа: обеспечение восприятия, осмысления и первичного закрепления учащимися форм записи алгоритма
Три состояния одного и того же вещества , в физике называют агрегатными состояниями данного вещества. Вода состоит из молекул.
-Чем же эти три состояния отличаются друг от друга?
Обучающиеся, отвечают на поставленный вопрос:
а) газообразное состояние : газы не имеют своего объёма и формы; занимают весь предоставленный объём; легко меняют объём.
б) жидкое состояние : легко меняет свою форму; принимает форму сосуда; объём трудно изменить.
в) твёрдое состояние : тело сохраняет форму и объём; трудно изменить форму и объём; молекулы сцеплены образуя цельную кристаллическую решётку.
Фиксируют запись в тетрадь.
Управление поведением партнера – контроль, коррекция, оценка действий партнера (К).
Рефлексия способов и условий действия (П).
Из выше сказанного мы с вами сделали выводы, а теперь зафиксируем в тетрадях основное положение молекулярно-кинетической теории
Основные положения МКТ
Все вещества состоят из мельчайших частиц.
Молекулы беспорядочно движутся.
Молекулы вещества взаимодействуют - притягиваютя и отталкиваются.
Ребята фиксируют запись в тетрадь.
Физкультминутка
Мы много писали, устали . Я буду давать команды, а вы их выполнять. Даются команды на активизацию мышц рук, головы, глаз и т.д. Например, посмотрите вверх; посмотрите на соседа слева; помашите соседу, сидящему за вами, и т.п.
Выполняют упражнения для двигательного аппарата, рук и глаз.
Умение слушать и слышать (К).
IV . Первичное закрепление
Цель этапа: проговаривание и закрепление нового знания; выявление пробелов первичного осмысления изученного материала, неверных представлений уч-ся; проведение коррекции.
Тест, Интерактивное задание Тест к уроку
Самостоятельно решают задачу, повторяя, систематизируя изученный материал.
Выбор наиболее эффективных способов решения задач в зависимости от конкретных условий (П).
Оценивание усваиваемого содержания (Л).
V . Итог урока (рефлексия деятельности)
Цель этапа : осознание уч-ся своей учебной деятельности, самооценка результатов деятельности своей и всего класса
Какую тему мы изучили на уроке?
Запах духов от источника распространится во всей комнате, или локально?
Вещество легко меняет свою форму, в каком состоянии оно находится?
Почему грецкий орех трудно бывает расколоть?
Пары бензина и жидкий бензин состоят из одинаковых или разных молекул?
Сравните давление в шинах автомобиля: на стоянке и при езде.
Какое волшебство позволяет воде быть в трёх различных состояниях?
Можно или нет: получить металлический пар?
Домашнее задание.
Откройте свои дневники и запишите домашнее задание.
Прочитать § 11-12, задание 3, стр.29
Учащиеся дают ответы на вопросы.
Называют основные позиции нового материала и как они их усвоили.
Различные состояния вещества и их объяснение на основе молекулярно-кинетических представлений
Запах духов от источника распространится во всей комнате.
Вещество находится в жидком состоянии.
Грецкий орех трудно расколоть – прочность кристаллической решётки.
Пары бензина и жидкий бензин состоят из одинаковых молекул.
Давление в шинах автомобиля: больше при езде, чем на стоянке.
Вода может находиться в 3-х состояниях из-за разной температуры.
Металлический пар образуется при нагревании расплавленного металла.
Записывают домашнее задание.
Рефлексия способов и условий действия; контроль и оценка процесса и результатов деятельности (П).
Самооценка; адекватное понимания причин успеха или неуспеха в УД; следование в поведении моральным нормам и этическим требованиям (Л).
Выражение своих мыслей полно и точно; формулирование и аргументация своего мнения, учет разных мнений (К).
1.Физика 7 класс: учебник для общеобразовательных учреждений/ А.В. Перышкин. - 16-е издание, доп.- М.: Дрофа, 2012
3.Лукашик В.И. Сборник задач по физике для 7-9 классов общеобразовательных учреждений – М.: Просвещение, 2011

Урок посвящён изучению агрегатных состояний веществ, физическим явлениям. Рассматриваются свойства и особенности строения аморфных веществ на конкретных примерах.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Агрегатные состояния веществ"
Все вещества при нормальных условиях могут находиться в трёх cсостояниях: твёрдом, жидком и газообразном. Такие состояния веществ называют агрегатными.
Например, при нормальных условиях вода находится в жидком агрегатном состоянии, при температуре 0 0 С вода находится в твёрдом агрегатном состоянии (это всем известный лёд). Ледяной узор на стекле, снег и гигантский айсберг – это всё твёрдое агрегатное состояние воды.
Если воду нагреть до температуры 100 0 С, то она переходит в газообразное состояние, так называемый пар. Этот пар представляет собой скопление мельчайших водяных капелек. Облака – это миллиарды мельчайших капелек воды.
Большинство газообразных веществ бесцветны, поэтому увидеть их невозможно. Находясь в сосуде, они принимают его форму. Объём газов зависит от температуры и давления, поэтому газы сжимаемы. Это свойство широко используется. Например, с помощью сжатого воздуха закрываются и открываются двери в автобусе, поток раскалённых газов реактивного двигателя поднимает ввысь самолёты, купол парашюта, наполненный упругим воздухом, позволяет плавно опуститься на землю.
Несомненно, переливать жидкости более привычно и наглядно. Если жидкость налить в сосуд, то она примет форму того сосуда, в который её налили. Это отражает такое свойство жидкости, как текучесть. Одни жидкости достаточно быстро растекаются по плоской поверхности, например, вода, спирт, бензин, ацетон. Другие жидкости – очень медленно. Так, капля мёда на стекле будет растекаться очень медленно, для того, чтобы это сделать, нужно стекло поставить вертикально. Жидкости, в отличие от газов, практически не сжимаются. Если хлопнуть по поверхности воды, то эффект будет таким же, как, если хлопнуть по крышке стола.
Если жидкость охладить, то она переходит в твёрдое агрегатное состояние. Твёрдые тела сохраняют свои объём и форму, они практически не сжимаются. Так, кубики льда постоянно буду иметь свои форму и объём, куда бы мы их не перемещали, пока они не растают.
Диффузию, броуновское движение, переход веществ из одного агрегатного состояния в другое относят к физическим явлениям, так как не происходит превращения одних веществ в другие.
Таким образом, физические явления – это явления, при которых изменяются агрегатные состояния веществ, форма и размеры тел, построенных из этого вещества, но сохраняется их химический состав.
В газообразных веществах расстояние между молекулами в десятки раз превышает размер самих молекул, поэтому они слабо связаны друг с другом и газы легко сжимаются. В твёрдых веществах частицы, из которых они состоят, находятся плотно друг к другу и в определённом порядке, как солдаты в строю. Такое упорядоченное строение частиц имеют кристаллы. Силы притяжения частиц в кристаллах велики, оторвать эти частицы очень непросто.
Жидкие вещества – это нечто промежуточное между газами и твёрдыми веществами.
Жидкости имеют объём, как и твёрдые вещества, расстояние между молекулами небольшое, но силы притяжения между частицами не так велики, как в кристаллах.
Есть ещё вещества, которые настолько вязкие, что долго сохраняют свою форму, как твёрдые вещества, однако расположение частиц в них неупорядоченное, как в жидкостях. Такие вещества называются аморфными. Аморфными веществами являются янтарь, воск, стекло, смолы, многие пластмассы.
Но как можно отличить кристаллическое вещество от аморфного? Если, например, нагреть стекло, то оно размягчится, потом становится текучим, пока не превратится в типичную жидкость. То есть резкой границы между аморфными веществами и жидкостями нет.
У каждого же твёрдого вещества есть определённая температура плавления, при которой оно переходит из твёрдого состояния в жидкое.

Понимают: основные положения МКТ, существование различных агрегатных состояний вещества.
Умеют: применять знания о строении и свойствах вещества к обоснованию закономерностей перехода от одного состояния в другое.
Ожидаемый результат: умеют объяснять строение веществ на основе МКТ
Гипотеза: Свойства веществ зависят от агрегатного состояния вещества и его молекулярного строения
На уроке используется опора для создания кластера, работа с таблицей, презентацией.
Используются элементы формативного оценивания. Учащиеся приходят к выводу:от движения молекул и от их взаимного расположения зависит, в каком агрегатном состоянии находится вещество.

Три положения МКТ
Отгадай загадки
- 1.В каком агрегатном состоянии Джин, если он без труда покидает кувшин?
- 2. Над рекой, над долиной повисла белая холстина.3. С неба пришел, в землю ушел.4. На всех садится, никого не боится5. Что в гору не выкатишь?6. Рассыпался горох на семьдесят дорог, никто его не подберет.
- 7. Белая скатерть всю землю покрыла.
- 8.Что вверх корнем растёт?
В каких состояниях находились вещества?

В природе вещества встречаются в трехсостояниях:

Тема: Агрегатные состояния вещества и объяснение их на основе молекулярно-кинетических представлений.

Свойства твердого тела
Твердое тело имеет собственную
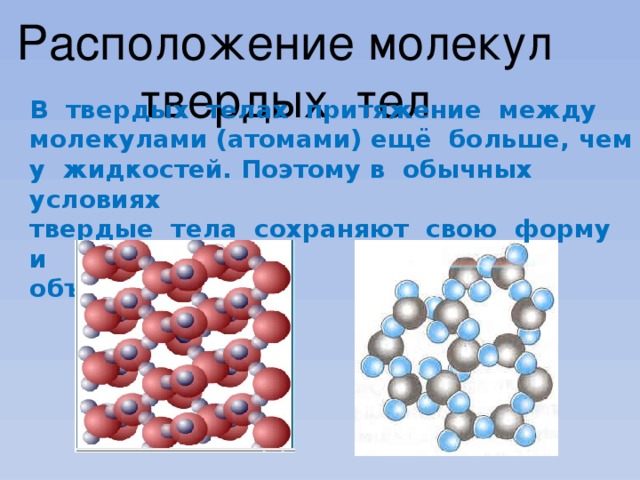
В твердых телах притяжение между
молекулами (атомами) ещё больше, чем
у жидкостей. Поэтому в обычных условиях
твердые тела сохраняют свою форму и
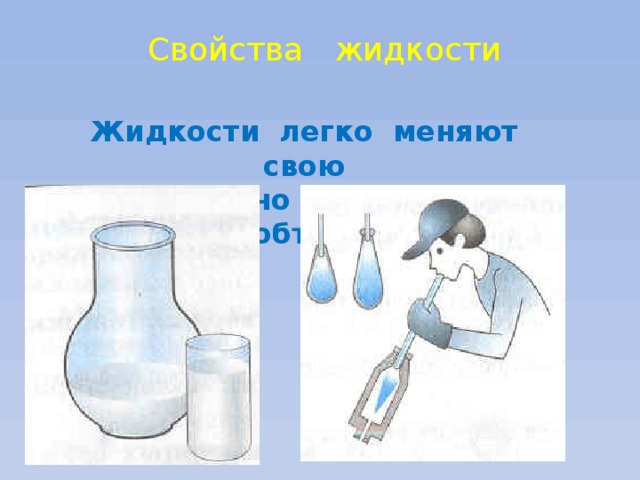
Жидкости легко меняют свою
форму, но сохраняют объем

Молекулы жидкости не расходятся на
большие расстояния, и жидкость в
обычных условиях сохраняет свой объем
Расположение молекул жидкости

Газы не имеют собственной формы и
постоянного объема. Они принимают форму сосуда и полностью заполняют
Читайте также:

