Биологические катализаторы конспект урока 9 класс биология
Обновлено: 05.07.2024
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Тема: Биологические катализаторы
I .Организационный момент
II . Проверка знаний
Понятийная разминка : биополимер, мономер, липиды, белки, глобула, денатурация, ренатурация, гликопротеины, липопротеины, нуклепротеины, ферменты, нуклеиновые кислоты, комплементарность, репликация, редупликация, АТФ, витамины, гипервитаминоз, гиповитаминоз, авитаминоз.
Биологический диктант.
III . Изучение нового материала
1. Катализаторы и их роль в химических реакциях. Ферменты — биокатализаторы. (Беседа.)
Катализаторы – вещества, изменяющие скорость химической реакции, но не входящие в состав продуктов реакции.
Ферменты – биологические катализаторы.
Фермент = белок + кофермент (небелковое соединение
2. Механизм действия ферментов. (Объяснение учителя с использованием таблицы и рисунка 14 учебника.)
Рис. 1. Схема ферментативной реакции
Е – фермент;
S – субстрат;
ES – комплекс “фермент–субстрат”;
Р1, Р2 – продукты реакции;
К1, К2, К3 – константы равновесия.
IV .Закрепление материала
Работа с вопросами на с.37 учебника
1. Выпишите буквы, обозначающие элементы верного ответа: какие функции в организме выполняют жиры?
A) откладываются в запас
Б) служат источником энергии
B) ускоряют химические реакции
Г) входят в состав клеточных мембран
Д) в печени могут превращаться в белки
Е) участвуют в хранении и передаче наследственных признаков от родителей к потомству
2. Выпишите буквы, обозначающие элементы верного ответа на вопрос: какие вещества подвергаются расщеплению в тонком кишечнике?
Д) минеральные соли
Е) нуклеиновые кислоты
3. Соотнесите виды химических связей со структурами белковых молекул, в которых они возникают.
Виды химических связей
Структуры белковой молекулы
Задания С из демо-2007
Белки и жиры – высокомолекулярные органические соединения. Молекула белка образованна большим числом аминокислот, в состав которых входят атомы углерода, водорода, кислорода, азота и серы. Жиры состоят из глицерина и жирных кислот. Они нерастворимы в воде, но хорошо растворимы в органических растворителях. В состав жиров входят атомы углерода, водорода и кислорода. Жиры и жироподобные вещества объединяются обычно под общим названием липиды. Как и углеводы, они служат источником энергии.
Белки разных клеток неодинаковы, специфичны. Однако они обладают общим свойством – свертываться при нагревании или воздействии ультрафиолетовых лучей. Белки являются основным строительным материалом любой клетки: входят в состав клеточных мембран, цитоплазмы, ядра и органоидов. Многие белки являются ферментами. У животных, все виды движения обеспечиваются сократительными белками. Вещества участвуют в защите клеток и контактах со средой. Некоторые белки выполняют транспортную функцию, присоединяя и перенося кислород и углекислый газ.
Жиры как белки выполняют ряд функций. Они входят в состав клеточных мембран и тем самым выполняют строительную функцию. Жиры могут накапливаться в клетках и служить запасным питательным веществом. Некоторые жироподобные вещества являются гормонами, принимая участие в регуляции физиологических функций организма.
Сравнительная характеристика белков и жиров
Признаки для сравнения
Строение молекул органических соединений
Свертываются при нагревании и действии ультрафиолетовых лучей
Растворяются только в органических растворителях
Сходные функции органических соединений
С 3. Элементы ответа:
1) 1 - Глицерин и жирные кислоты
3) 3 - Строительная функция
С 4. Элементы ответа:
1) Название клеточной структуры - клеточная мембрана
2) отграничивает клетку от окружающей среды
3) обеспечивают избирательное поступление и выделение веществ.
С 5. Элементы ответа:
2) Отсутствие белков приведет к тому, что в клетках не будут выполняться следующие функции: ферментативная, двигательная, защитная, транспортная.
3) Синтез белков из жиров невозможен, т.к. белки имеют более сложное строение (их молекулы включают азот и серу).
V .Задание на дом

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Биологические катализаторы"
Начнём с цитаты известного советского химика и инженера, академика Георгия Константиновича Борескова:
Неуютная картина, не правда ли? Поэтому сегодняшняя наша цель – разобраться, почему же Земля всё-таки выглядит более привычно для нашего глаза.

Для протекания многих химических реакций необходимы специальные условия. Чаще всего на скорость реакций влияют температура и давление. Чем они выше, тем быстрее протекает химическая реакция. Но её скорость можно увеличить, не изменяя внешних условий, а просто добавив к реагирующей смеси определённые вещества. Так, металлический родий почти в 10000 раз ускоряет разложение муравьиной кислоты на углекислый газ и водород. Такие вещества, увеличивающие скорость реакции, но не входящие в состав продуктов реакции, называются катализаторами.
В клетках живых организмов каждую секунду происходят тысячи химических реакций.
И это несмотря на то, что в живой клетке умеренная температура и нормальное давление. Например, бактерии из рода Азотобактер могут при обычных условиях разрывать прочнейшую молекулу азота, где атомы соединены тремя ковалентными связями и присоединять их к водороду. А для того, чтобы проделать то же самое человеку в промышленности, необходимо создать давление в 350 раз большее, чем на поверхности Земли и поднять температуру до 500 градусов Цельсия.
Естественно, бактерии не обходятся при этом без катализаторов. Кстати, люди также пытались применить их при получении аммиака. Перепробовав при этом более 20000 различных веществ.
Что же за всесильные вещества – эти катализаторы?
Катализаторами химических реакций в неживой природе могут быть самые различные вещества. Это и уже упомянутый нами экзотический родий, который используется для изготовления зеркал супермощных лазеров и обычный оксид марганца, применяемый для получения кислорода даже в школьной лаборатории.
Кроме того, неорганические катализаторы могут ускорять реакции с разными веществами. Например, родий не только эффективно разлагает муравьиную кислоту, но и борется с выбросами вредных оксидов азота в автомобильных катализаторах.
Другое дело – биологические, а значит, органические катализаторы. На них мы остановимся более подробно.
Многочисленные исследования прошлого нашей планеты говорят о том, что на начальном этапе зарождения жизни каталитической способностью обладали некоторые молекулы рибонуклеиновых кислот.

И тогда это свойство РНК имело очень важное значение. Сегодня же роль молекул РНК как катализаторов крайне мала. А основными биокатализаторами в клетке являются ферменты. Которых уже к 2013 году было описано более пяти тысяч видов.
Абсолютно все процессы в живом организме прямо или косвенно осуществляются с участием ферментов или энзимов, как их ещё называют. Это и фиксация углерода в процессе фотосинтеза, и расщепление питательных веществ в пищеварительном тракте, и синтез источника энергии для всех живых организмов – АТФ, и многое –многое другое.
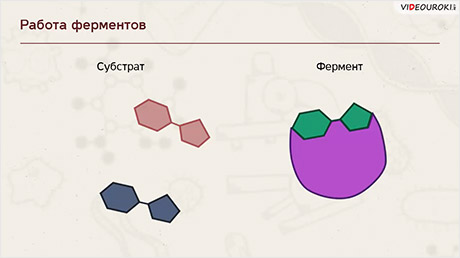
Как вы помните, по химической природе биологические катализаторы относятся к белкам. Они могут быть как простыми, состоящими только из аминокислот, так и сложными, включающими белок и небелковую часть – простетическую группу. Простетическая группа фермента называется кофермент, а белковая часть – апофермент.
В роли коферментов выступают органические и неорганические вещества. Среди органических это могут быть витамины, например, аскорбиновая кислота. А из неорганических – ионы различных металлов. Например, ионы меди, железа, магния.
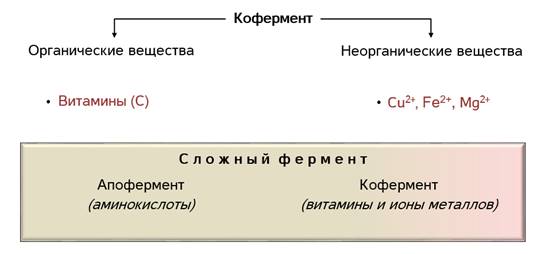
Ферменты ускоряют химические реакции за счёт тесного взаимодействия с молекулами исходных реагирующих веществ – так называемых субстратов. Зачастую размеры молекул субстратов значительно меньше размеров молекул самих ферментов, хотя, казалось бы, должно быть наоборот. Поэтому с субстратом или субстратами, потому что их может быть несколько, взаимодействует не вся молекула фермента, а лишь небольшой её участок – активный центр фермента. Построен он чаще всего из нескольких аминокислотных остатков, которые образуют его уникальную структуру. Почему уникальную? Дело в том, что форма и химическое строение активного центра таковы, что с ним могут связываться только те субстраты, структура которых подходит к структуре активного центра.
Магия этого процесса неизвестна до сих пор. Несмотря на то, что человечество в ближайшее время планирует полёты на Марс, оно не в состоянии разобраться со своим организмом. Но существует теория. Её выдвинул ещё в 1890 году немецкий химик Эмиль Фишер.
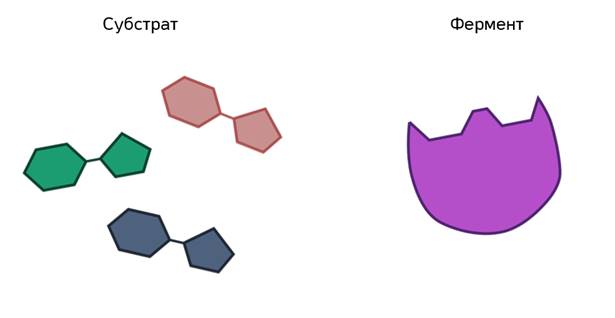
В этом комплексе молекула субстрата деформируется и в её структуре ослабляются определённые химические связи. Что приводит к облегчённому их разрыву и в конечном итоге к ускорению химической реакции.
После этого фермент-субстратный комплекс распадается на конечные продукты и свободный фермент, а активный центр последнего тут же готов принимать новые молекулы субстрата. Получаем такой же итог, как и в случае работы обычных химических катализаторов – скорость реакции увеличивается, а сам катализатор при этом не расходуется и может использоваться многократно.
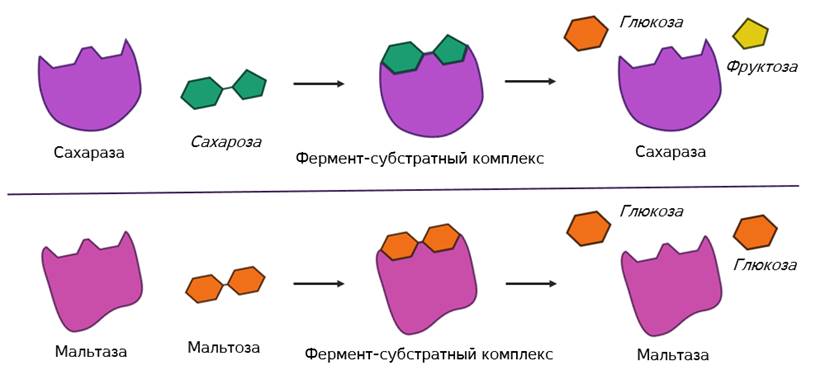
Но в самом механизме работы органических и неорганических катализаторов есть кардинальное отличие. Каждый фермент действует только на определённый тип связи и ускоряет только одну определённую реакцию. То есть обладает специфичностью. Как вы поняли, специфичность объясняется соответствием активного центра только определённым субстратам. Поэтому, например, фермент мальтаза, разлагающий дисахарид мальтозу до двух молекул глюкозы оказывается не способным разрушать молекулы сахарозы. Несмотря на то, что сахароза также является дисахаридом.
Активирующее влияние на скорость ферментативной реакции оказывают разнообразные вещества органической и неорганической природы. Например, в желудке человека соляная кислота активирует фермент пепсин. Максимальная активность которого лежит в пределах рН от полутора до двух.
Ингибирование ферментов может быть обратимым и необратимым. Если вещество-ингибитор вызывает стойкое изменение пространственной структуры фермента, то такое ингибирование будет необратимым.
А вот обратимое ингибирование, в свою очередь, бывает двух типов. Давайте их рассмотрим.
С активным центром фермента могут связываться вещества, сходные по структуре с субстратом. Никакой реакции при этом нет, но между ингибиторами и субстратом происходит конкуренция за активный центр. Поэтому такой тип ингибирования называется конкурентным.
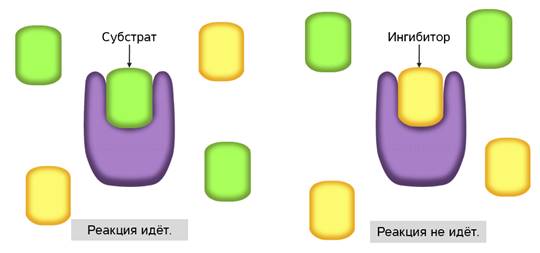
Конкурентное ингибирование широко используется в медицине. Антибиотики, противоопухолевые препараты, используемые в качестве лекарственных средств, являются конкурентными ингибиторами.
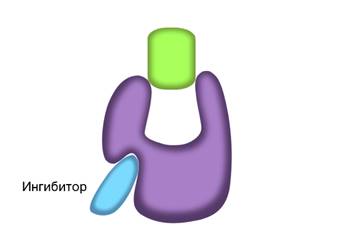
В неконкурентном ингибировании не участвуют вещества, сходные с субстратом. При таком типе ингибирования, молекулы ингибиторов присоединяются к регуляторному центру фермента. Это вызывает изменение пространственной структуры активного центра, что препятствует присоединению к нему молекул субстрата. Тем самым снижается скорость ферментативной реакции.
Уникальные способности ферментов уже много лет используются человеком в хозяйственной деятельности. В настоящее время развивается новая отрасль науки – промышленная энзимология. Которая, в свою очередь, является основой биотехнологии.
Мы уже упоминали об использовании ферментов в медицине. Фармацевтическая промышленность научилась производить искусственный аналог гормона надпочечников кортизола – преднизолон. Который используется при лечении ревматоидного артрита.
Широкое применение ферменты-энзимы находят также в пищевой промышленности. Их применяют в производстве сыров, соков, овощных и фруктовых пюре. Не обходится без применения ферментов хлебопечение, производство алкогольных напитков. Для улучшения вкуса, аромата и консистенции их применяют для обработки мяса.
В текстильной и кожевенной промышленности ферменты позволяют значительно увеличить выход овчины, а обработка кожи перед дублением делает её поверхность чистой, гладкой и тонкой.
Перспективным является применение ферментов, разлагающих целлюлозу. В результате этого из древесины, торфа, сельскохозяйственных и городских отходов можно получить ценные биотехнологические продукты: глюкозу, этанол, ацетон и другие. Особую актуальность это имеет в наши дни, когда проблема загрязнения окружающей среды выходит на передний план.

Урок для учащихся девятого класса. На уроке учащиеся с знакомятся с понятиями катализатор, катализ, ферменты. В ходе урока выполняется лабораторная работа, где ребята в сравнении рассматривают действие фермента на системы. Решают задачи на состав и процентное отношение нуклеотидов в составе ДНК. Делают выводы о значении биологических катализаторов - ферментов.
Биологические катализаторы
(урок в 9 классе).
Тема урока: Биологические катализаторы.
Сформировать знания о ферментах , их роли в клетке.
Активизировать знания о катализе, катализаторах из курса химии.
Оборудование: 3% - раствор перекиси водорода, кусочки сырого и вареного картофеля и мяса, пробирки.
Тип урока: комбинированный.
Организационный момент.
Объявление темы и целей занятия.
Проверка знаний.
Решение биологических задач.
АТФ – постоянный источник энергии для клетки. Его роль можно сравнить с ролью аккумулятора. Объясните, в чем заключается это сходство.
АТФ синтезируется в митохондриях и хлоропластах. Объясните, в чем сходство и различие процессов, приводящих к синтезу молекул в органоидах.
Дано: Т = 880 – 22%.
Найти: 1) А, Г, Ц всего и в %;
Находим общее количество нуклеотидов.
Г+Ц= 4000 – (880+880)= 2240.
Находим длину ДНК.
4000:2∙0,34 нм = 680 нм.
Ответ: а)А=880 – 22%
Изучение нового материала.
Проблемный вопрос: Какие вещества называются катализаторами и какова их роль в химических реакциях.
Катализ (рассказ с элементами беседы).
Катализ – явление ускорения реакции без изменения её общего результата (стр. 35).
Катализаторы – вещества, изменяющие скорость химической реакции, но не входящие в состав продуктов реакции.
Ферменты – биологические катализаторы.
Фермент каталаза имеется в каждой растительной и животной клетке. Он расщепляет Н2О2, которая образуется в клетках в результате окислительно-восстановительных реакций. С появлением молекул воды и кислорода:
За 1 секунду 1 молекула каталазы расщепляет 200000 молекул Н 2О 2
Н 2О 2 – ядовитое вещество, и чтобы не произошло самоотравления клетки и организма в целом, каталаза расщепляет её.

7. Какой из видов молекул РНК имеет самые длинные цепочки?
8. Какой вид РНК вступает в реакцию с аминокислотами?
9. Какие нуклеотиды входят в состав РНК?
10.Найдите соответствие нуклеиновым кислотам:
Признаки соответствия кислот
2. Мономеры фосфорная кислота, углевод, азотистое основание
8. Нуклеотиды: аденин,урацил ,гуанин,цитозин
9.Больше всего находится в ядре -99%
10.Находится в ядрышках,рибососмах,цитоплазме
11.Образуют более длинные цепочки
12. Образуют короткие цепочки
Карточка №1.6 Ответы:
3) Остаток фосфорной кислоты, дезоксирибоза, аденин
4) Снятие и перенос информации с ДНК
6) Остаток фосфорной кислоты и сахарами соседних нуклеотидов
9) Аденин, урацил, гуанин, цитозин.
Урок № 8. Тема: «АТФ и другие органические соединения клетки.
Цель урока: изучить строение АТФ .
1. Обучающие:
познакомить учащихся со строением и функциями молекулы АТФ;
познакомить с другими органическими соединениями клетки.
научить школьников расписывать гидролиз перехода АТФ в АДФ, АДФ в АМФ;
2. Развивающие:
сформировать у учащихся личностную мотивацию, познавательный интерес к данной теме;
расширить знания о энергии химических связей и витаминах
развить интеллектуальные и творческие способности учащихся, диалектическое мышление;
углубить знания о взаимосвязи строения атома и структурой ПСХЭ;
отработать навыки образования АМФ из АТФ и наоборот.
3. Воспитательная:
продолжить развивать познавательный интерес строения элементов молекулярного уровня любой клетки биологического объекта.
сформировать толерантное отношение к своему здоровью, зная какую роль играют витамины в организме человека.
Оборудование: таблица, учебник, мультимедийный проектор.
Тип урока: комбинированный
I . Организационный момент.
II . Проверка знаний
Понятийная разминка: биополимер, мономер, мальтоза, сахароза, лактоза, липиды, белки, глобула, денатурация, ренатурация, гликопротеины, липопротеины, нуклепротеины, ферменты, нуклеиновые кислоты, комплементарность, репликация, редупликация.
Строение ДНК и РНК.
Построение второй цепочки ДНК. (Работа с динамической моделью или с дидактическими карточками.)
Какой из нуклеотидов не входит в состав ДНК?
Если нуклеотидный состав ДНК –АТТ-ГЦГ-ТАТ-, то каким должен быть нукеотидный состав и-РНК?
Укажите состав нуклеотида ДНК?
Какую функцию выполняет и-РНК?
Что является мономерами ДНК и РНК?
Назовите основные отличия и-РНК от ДНК.
Прочная ковалентная связь в молекуле ДНК возникает между: …
Какой из видов молекул РНК имеет самые длинные цепочки?
Какой вид РНК вступает в реакцию с аминокислотами?
Какие нуклеотиды входят в состав РНК?
Остаток фосфорной кислоты, дизоксирибоза, аденин
Снятии и перенос информации с ДНК
Одноцепочная, содержит рибозу, передает информацию.
Остаток фосфорной кислоты и сахарами соседних нуклеотидов
Аденин, урацил, гуанин, цитозин.
5.Повторение изученного материала( решение биологических задач),
- работа у доски 2 обучающихся, остальные работают на карточках
Задача 1. В молекуле ДНК обнаружено 880 гуаниловых нуклеотидов, которые составляют 22% от общего количества нуклеотидов этой ДНК.
Определите: а) сколько содержится других нуклеотидов (по отдельности) в этой молекуле ДНК
б) какова длина ДНК
На основе принципа комплементароности
1.Определяем количество второго (цитидилового) нуклеотида:
2.На долю других видов нуклеотидов (Т+А) приходится
3.Для вычисления количества этих нуклеотидов составляем пропорцию:
X = (56 x 880) : 22= 2240
2240 : 2 вида нуклеотида = 1120 А, столько же Т.
Всего 880 + 880 + 1120 = 4000 нуклеотидов
4.Для определения длины ДНК, сколько нуклеотидов содержится в одной цепи :
5.Вычисляем длину цепи 2000 x 0,34 = 680нм
Такова длина и всей молекулы ДНК
Ответ : а) Г=Ц=880; А=Т=1120; б) 680 нм
Самостоятельная работа
Дано: А нукл. = 600 = 12,5%
Найти: а) Т,Г,Ц всего и в %
Дано: Цнукл. = 300 = 15%
Найти: а) Г, Т, А всего и в %
III . Изучение нового материала.
Кинетическая, потенциальная - эти виды энергии вы изучали на уроках физики . В биологии тоже есть свой вид энергии - энергия химических связей. Предположим, вы выпили чай с сахаром. Пища поступила в желудок, там разжижается и направляется в тонкий кишечник, где идет её расщепление: крупные молекулы до мелких. Т.е. сахар-это углевод дисахарид, который расщепляется до глюкозы. Она расщепляется и служит источником энергии, т.е.50%энергии рассеивается в виде теплоты для поддержания постоянной t тела, и 50% энергии, которая превращается в энергию АТФ, она хранится для нужд клетки.
Итак, цель урока - изучить строение молекулы АТФ.
Кроме Б,Ж,У,НК в клетках находятся другие органические соединения. Их можно условно разделить на конечные, промежуточные и распада.
Рассмотрим конечное органическое соединение- АТФ.
Строение АТФ и ее роль в клетке.
АТФ был открыт в 1929 г. Карлом Ломанном, а в 1941 году Фриц Липман показал, что АТФ является основным переносчиком энергии в клетке.
АТФ - аденозинтрифосфат - нуклеотид, состоящий из азотистого основания аденина, углевода рибозы и 3-х остатков Н3РО4, соединенных поочередно.
Функция АТФ
АТФ - играет исключительно важную роль в обмене энергии и веществ в организмах,это универсальный источник энергии.
АТФ-универсальный биологический аккумулятор энергии.Световая энергия солнца и энергия, заключенная в потребляемой пище, запасается в молекулах АТФ.
АТФ содержится в цитоплазме, митохондриях, ядре.

- Р – Р - Р
Три остатка фосфорной
Это интересно!
Продолжительность жизни одной молекулы АТФ у человека менее 1 мин.
Человеческий организм синтезирует около 40 кг АТФ в день.
Энергетическая эффективность двух макроэргических связей составляет 80 кДж/моль
АТФ-это неустойчивая структура. Если отделить 1 остаток НЗР04, то АТФ перейдет в АДФ:
АТФ+Н2О =АДФ+Н3РО4+Е, Е=40кДж , где Е-освобождающаяся энергия
Если освобождается еще один остаток фосфорной кислоты,то АДФ переходит в аденозинмонофосфат – АМФ.
При отделении каждого остатка фосфорной кислоты освобождается 40 кДж энергии.
АДФ + Н2О = АМФ+Н3РО4+Е, Е=40кДж
Связь между остатками фосфорной кислоты называют макроэргической (обозначают символом ),так при разрыве выделяется в 4 раза больше энергии.
Витамины и другие органические соединения клетки.
Кроме изученных органических соединений (белки, жиры, углеводы) есть органические соединения- витамины. Вы едите овощи, фрукты, мясо? (Да, конечно!)
Все эти продукты содержат большое количество витаминов. Для нормального функционирования нашего организма витаминов, поступающих с пищей, нужно небольшое количество. Но не всегда тот объём продуктов, который мы употребляем, способен восполнить наш организм витаминами. Одни витамины организм может синтезировать сам, другие же поступают только с пищей (н., витамин К, С).
Витамины – группа низкомолекулярных органических соединений относительно простого строения и разнообразной химической природы.
Все витамины принято обозначать буквами латинского алфавита-А, В, D, F.
По растворимости в воде и в жирах витамины делят на:
Витамины участвуют во множестве биохимических реакций, выполняя каталитическую функцию в составе активных центров большого количества разнообразных ферментов.
Витаминам отводится важнейшая роль в обмене веществ. Концентрация витаминов в тканях и суточная потребность в них невелики, но при недостаточном поступлении витаминов в организм наступают характерные и опасные патологические изменения.
Большинство витаминов не синтезируются в организме человека, поэтому они должны регулярно и в достаточном количестве поступать в организм с пищей или в виде витаминно-минеральных комплексов и пищевых добавок.
С нарушением поступления витаминов в организм связаны два принципиальных патологических состояния:
Гиповитаминоз – недостаток витамина.
Гипервитаминоз – избыток витамина.
Авитаминоз – полное отсутствие витамина.
Закрепление знаний об АТФ
- решение биологических задач
АТФ – постоянный источник энергии для клетки. Его роль можно сравнить с ролью аккумулятора. Объясните, в чем заключается это сходство.
АТФ синтезируются в митохондриях и хлоропластах. Объясните, в чем сходство и различие процессов, приводящих к синтезу молекул в органоидах.
I V. Закрепление материала
Как устроена молекула АТФ?
Какое значение играет АТФ в организме?
Как образуется АТФ?
Почему связи между остатками фосфорной кислоты называются макроэргическими?
Что нового вы узнали о витаминах?
Зачем нужны витамины в организме?
V. Задание на дом
- Сформировать знания о ферментах , их роли в клетке.
- Активизировать знания о катализе, катализаторах из курса химии.
Задачи:
-сформировать у учащихся знания о биологических катализаторах, выяснить особенности строения и механизма действия, их значение;
- способствовать обучению учащихся умению анализировать, делать выводы, на основе практических действий добывать знания;
- продолжить воспитание убежденности в возможности познания закономерностей живой природы.
Тип урока: комбинированный.
Организационный момент.
Объявление темы и целей занятия.
Проверка знаний.
Решение биологических задач.
АТФ – постоянный источник энергии для клетки. Его роль можно сравнить с ролью аккумулятора. Объясните, в чем заключается это сходство.
АТФ синтезируется в митохондриях и хлоропластах. Объясните, в чем сходство и различие процессов, приводящих к синтезу молекул в органоидах.
Дано: Т = 880 – 22%.
Найти: 1) А, Г, Ц всего и в %;
Находим общее количество нуклеотидов.
Г+Ц= 4000 – (880+880)= 2240.
Находим длину ДНК.
4000:2∙0,34 нм = 680 нм.
Ответ: а)А=880 – 22% Г+Ц= 1120 – 28%
Изучение нового материала.
Проблемный вопрос: Какие вещества называются катализаторами и какова их роль в химических реакциях.
Катализ (рассказ с элементами беседы).
Практически все
Катализ – явление ускорения реакции без изменения её общего результата (стр. 35). Вы знаете, что для протекания многих химических реакций необходимы высокие температура и давление. В то же время при добавлении к реагирующей смеси определенных веществ та же реакция может протекать даже при нормальных условиях и с большей скоростью.
Какие вещества называются катализаторами?
Катализаторы – вещества, изменяющие скорость химической реакции, но не входящие в состав продуктов реакции
Какие мы знаем вещества, ускоряющие реакции? - Ферменты.
Ферменты – биологические катализаторы.
Пример. Рассмотрим реакцию, знакомую всем владельцам кошек. Фермент уреаза разлагает мочевину. Речь идёт о разложении мочевины, содержащейся в кошачьей моче, на углекислый газ и аммиак(именно аммиаком пахнет кошачий ящик с песком).
Уреазу образуют бактерии, попавшие в песок из воздуха. Одна молекула уреазы за 1 секунду расщепляет 30 000 молекул мочевины. Без катализатора эта реакция шла бы 3000 000 лет.
1897 год - Эдуард Бухнер выделил комплекс ферментов.
1926 год - Дж. Самнер обнаружил, что ферменты – белки.
В живой клетке умеренная температура, нормальное давление. В таких условиях большинство реакций или вообще не протекали бы или протекали бы очень медленно, если бы не подвергались воздействию катализаторов.
Каталитической способностью обладают некоторые молекулы РНК. Очевидно, это свойство РНК имело очень важное значение на начальном этапе зарождения жизни на нашей планете. В настоящее время роль молекул РНК как катализаторов крайне мала, а основными биокатализаторами в клетке являются ферменты.
Какие ферменты нашего организма вам известны? Липаза, пепсин, амилаза, мальтаза…
Ферменты – это специфические белки, которые присутствуют во всех живых организмах и играют роль биологических катализаторов.
Строение и механизм действия ферментов.
Все процессы в живом организме прямо или косвенно осуществляются с участием ферментов. Сейчас уже известны тысячи ферментов. Молекулы одних ферментов состоят только из белков, другие включают белок и небелковое соединение, или кофермент. Кофермент – это небелковое соединение в виде витаминов или ионов различных металлов, входящее в состав фермента. В качестве коферментов выступают различные органические вещества, как правило, витамины, и неорганические — ионы различных металлов.
Свойства ферментов :
- участвуют в процессах синтеза и распада;
- действуют в строго определенной последовательности;
- специфичны для каждого вещества;
- ускоряют только определенные реакции
Ферменты действуют в строго определенной последовательности, они специфичны для каждого вещества и ускоряют только определенные реакции. Встречаются ферменты, которые катализируют несколько реакций. Избирательность действия ферментов на разные химические вещества связана с их строением.
У некоторых ферментов в присутствии молекул определенных веществ конфигурация активного центра может изменяться, т.е. фермент таким образом может обеспечить наибольшую ферментативную активность.
Факторы, влияющие на функционирование ферментов:
- природа и концентрация фермента и вещества;
- температура (свыше 60 о ферменты не функционируют)
- давление;
- реакции среды (кислая, нейтральная, щелочная).
Ферменты увеличивают скорость химических реакций в тысячи и миллионы раз. Но скорость ферментативных реакций зависит от многих факторов — природы и концентрации фермента и вещества, температуры, давления, реакции среды и т. д. Для функционирования каждого фермента имеются оптимальные условия. Например, одни ферменты активны в нейтральной, другие — в кислой или щелочной среде. При температуре свыше 60 °С большинство ферментов не функционирует.
Значение ферментов.
Ферменты используются в медицине для обработки ран, при лечении болезней газ и кожный болезней, ожогов, в урологии, при истощении, ожирении, при производстве антибиотиков, виноделии, хлебопечении, синтезе витаминов
Закрепление нового материала.
Теперь вы познакомитесь с действием ферментов, содержащихся в клетках, на практике. Записывайте в тетради – лабораторная работа. На столах у вас имеются карты-инструкции для выполнения лабораторной работы. Записывайте тему л/р, цель работы, оборудование. Ознакомьтесь с теоретическими основами и приступайте к выполнению работы.
- Что вы наблюдаете после того как прилили в пробирки пероксид водорода?
Пероксид водорода— нестойкое вещество, и даже в пробирке оно медленно расщепляется на воду и кислород. В пробирке с вареным картофелем никаких заметных изменений с пероксидом водорода не произошло, а в пробирке с сырым- энергично выделяются пузырьки кислорода.
- Почему в живых клетках пероксид водорода так бурно расщепляется, вспомните, как добиваются ускорения химических реакций?
В клетке содержатся катализаторы — ферменты, вызывающие значительное ускорение биохимических процессов.
Мы уже говорили, что при нагревании молекулы белка разрушаются, поэтому фермент перестает функционировать. Это было видно в опыте с мертвыми клетками. Теперь вам остается сформулировать вывод.
Читайте также:

