Роль альвеолярного сурфактанта в процессе дыхания кратко
Обновлено: 04.07.2024
Процесс дыхания, поступление кислорода в организм при вдохе и удаление из него углекислого газа и паров воды при выдохе. Строение респираторной системы. Ритмичность и различные типы дыхательного процесса. Регуляция дыхания. Разные способы дыхания.
Для нормального протекания обменных процессов в организме человека и животных в равной мере необходим как постоянный приток кислорода, так и непрерывное удаление углекислого газа, накапливающегося в ходе обмена веществ. Такой процесс называется внешним дыханием.
Дыхание – это совокупность процессов, обеспечивающих потребление организмом кислорода и выделение углекислого газа.
Таким образом, дыхание – одна из важнейших функций регулирования жизнедеятельности человеческого организма. В организме человека функцию дыхания обеспечивает дыхательная (респираторная система).
В дыхательную систему входят легкие и респираторный тракт (дыхательные пути), который, в свою очередь, включает носовые ходы, гортань, трахею, бронхи, мелкие бронхи и альвеолы (смотри рисунок 1.5.3). Бронхи разветвляются, распространяясь по всему объему легких, и напоминают крону дерева. Поэтому часто трахею и бронхи со всеми ответвлениями называют бронхиальным деревом.
Кислород в составе воздуха через носовые ходы, гортань, трахею и бронхи попадает в легкие. Концы самых мелких бронхов заканчиваются множеством тонкостенных легочных пузырьков – альвеол (смотри рисунок 1.5.3).
Альвеолы – это 500 миллионов пузырьков диаметром 0,2 мм, где происходит переход кислородом в кровь, удаление углекислого газа из крови.
Здесь и происходит газообмен. Кислород из легочных пузырьков проникает в кровь, а углекислый газ из крови – в легочные пузырьки (рисунок 1.5.4).
Рисунок 1.5.4. Легочный пузырек. Газообмен в легких
Важнейший механизм газообмена – это диффузия, при которой молекулы перемещаются из области их высокого скопления в область низкого содержания без затраты энергии (пассивный транспорт). Перенос кислорода из окружающей среды к клеткам производится путем транспорта кислорода в альвеолы, далее в кровь. Таким образом, венозная кровь обогащается кислородом и превращается в артериальную. Поэтому состав выдыхаемого воздуха отличается от состава наружного воздуха: в нем содержится меньше кислорода и больше углекислого газа, чем в наружном, и много водяных паров (смотри рисунок 1.5.4). Кислород связывается с гемоглобином, который содержится в эритроцитах, насыщенная кислородом кровь поступает в сердце и выталкивается в большой круг кровообращения. По нему кровь разносит кислород по всем тканям организма. Поступление кислорода в ткани обеспечивает их оптимальное функционирование, при недостаточном же поступлении наблюдается процесс кислородного голодания (гипоксии).
Недостаточное поступление кислорода может быть обусловлено несколькими причинами как внешними (уменьшение содержания кислорода во вдыхаемом воздухе), так и внутренними (состояние организма в данный момент времени). Пониженное содержание кислорода во вдыхаемом воздухе, так же как и увеличение содержания углекислого газа и других вредных токсических веществ наблюдается в связи с ухудшением экологической обстановки и загрязнением атмосферного воздуха. По данным экологов только 15% горожан проживают на территории с допустимым уровнем загрязнения воздуха, в большинстве же районов содержание углекислого газа увеличено в несколько раз.
При очень многих физиологических состояниях организма (подъем в гору, интенсивная мышечная нагрузка), так же как и при различных патологических процессах (заболевания сердечно-сосудистой, дыхательной и других систем) в организме также может наблюдаться гипоксия.
Природа выработала множество способов, с помощью которых организм приспосабливается к различным условиям существования, в том числе к гипоксии. Так компенсаторной реакцией организма, направленной на дополнительное поступление кислорода и скорейшее выведение избыточного количества углекислого газа из организма является углубление и учащение дыхания. Чем глубже дыхание, тем лучше вентилируются легкие и тем больше кислорода поступает к клеткам тканей.
К примеру, во время мышечной работы усиление вентиляции легких обеспечивает возрастающие потребности организма в кислороде. Если в покое глубина дыхания (объем воздуха, вдыхаемого или выдыхаемого за один вдох или выдох) составляет 0,5 л, то во время напряженной мышечной работы она увеличивается до 2-4 л в 1 минуту. Расширяются кровеносные сосуды легких и дыхательных путей (а также дыхательных мышц), увеличивается скорость тока крови по сосудам внутренних органов. Активируется работа дыхательных нейронов. Кроме того, в мышечной ткани есть особый белок (миоглобин), способный обратимо связывать кислород. 1 г миоглобина может связать примерно до 1,34 мл кислорода. Запасы кислорода в сердце составляют около 0,005 мл кислорода на 1 г ткани и этого количества в условиях полного прекращения доставки кислорода к миокарду может хватить для того, чтобы поддерживать окислительные процессы лишь в течение примерно 3-4 с.
Миоглобин играет роль кратковременного депо кислорода. В миокарде кислород, связанный с миоглобином, обеспечивает окислительные процессы в тех участках, кровоснабжение которых на короткий срок нарушается.
В начальном периоде интенсивной мышечной нагрузки увеличенные потребности скелетных мышц в кислороде частично удовлетворяются за счет кислорода, высвобождающегося миоглобином. В дальнейшем возрастает мышечный кровоток, и поступление кислорода к мышцам вновь становится адекватным.
Все эти факторы, включая усиление вентиляции легких, компенсируют кислородный “долг”, который наблюдается при физической работе. Естественно, увеличению доставки кислорода к работающим мышцам и удалению углекислого газа способствует согласованное увеличение кровообращения в других системах организма.
Саморегуляция дыхания. Организм осуществляет тонкое регулирование содержания кислорода и углекислого газа в крови, которое остается относительно постоянным, несмотря на колебания количества поступающего кислорода и потребности в нем. Во всех случаях регуляция интенсивности дыхания направлена на конечный приспособительный результат – оптимизацию газового состава внутренней среды организма.
Частота и глубина дыхания регулируются нервной системой – ее центральными (дыхательный центр) и периферическими (вегетативными) звеньями. В дыхательном центре, расположенном в головном мозге, имеются центр вдоха и центр выдоха.
Дыхательный центр представляет совокупность нейронов, расположенных в продолговатом мозге центральной нервной системы.
При нормальном дыхании центр вдоха посылает ритмические сигналы к мышцам груди и диафрагме, стимулируя их сокращение. Ритмические сигналы образуются в результате спонтанного образования электрических импульсов нейронами дыхательного центра.
Сокращение дыхательных мышц приводит к увеличению объема грудной полости, в результате чего воздух входит в легкие. По мере увеличения объема легких возбуждаются рецепторы растяжения, расположенные в стенках легких; они посылают сигналы в мозг – в центр выдоха. Этот центр подавляет активность центра вдоха, и поток импульсных сигналов к дыхательным мышцам прекращается. Мышцы расслабляются, объем грудной полости уменьшается, и воздух из легких вытесняется наружу (смотри рисунок 1.5.5).
Рисунок 1.5.5. Регуляция дыхания
Процесс дыхания, как уже отмечалось, состоит из легочного (внешнего) дыхания, а также транспорта газа кровью и тканевого (внутреннего) дыхания. Если клетки организма начинают интенсивно использовать кислород и выделять много углекислого газа, то в крови повышается концентрация угольной кислоты. Кроме того, увеличивается содержание молочной кислоты в крови за счет усиленного образования ее в мышцах. Данные кислоты стимулируют дыхательный центр, и частота и глубина дыхания увеличиваются. Это еще один уровень регуляции. В стенках крупных сосудов, отходящих от сердца, имеются специальные рецепторы, реагирующие на понижение уровня кислорода в крови. Эти рецепторы также стимулируют дыхательный центр, повышая интенсивность дыхания. Данный принцип автоматической регуляции дыхания лежит в основе бессознательного управления дыханием, что позволяет сохранить правильную работу всех органов и систем независимо от условий, в которых находится организм человека.
Ритмичность дыхательного процесса, различные типы дыхания. В норме дыхание представлено равномерными дыхательными циклами “вдох – выдох” до 12-16 дыхательных движений в минуту. В среднем такой акт дыхания совершается за 4-6 с. Акт вдоха проходит несколько быстрее, чем акт выдоха (соотношение длительности вдоха и выдоха в норме составляет 1:1,1 или 1:1,4). Такой тип дыхания называется эйпноэ (дословно – хорошее дыхание). При разговоре, приеме пищи ритм дыхания временно меняется: периодически могут наступать задержки дыхания на вдохе или на выходе (апноэ). Во время сна также возможно изменение ритма дыхания: в период медленного сна дыхание становится поверхностным и редким, а в период быстрого – углубляется и учащается. При физической нагрузке за счет повышенной потребности в кислороде возрастает частота и глубина дыхания, и, в зависимости от интенсивности работы, частота дыхательных движений может достигать 40 в минуту.
При смехе, вздохе, кашле, разговоре, пении происходят определенные изменения ритма дыхания по сравнению с так называемым нормальным автоматическим дыханием. Из этого следует, что способ и ритм дыхания можно целенаправленно регулировать с помощью сознательного изменения ритма дыхания.
Человек рождается уже с умением использовать лучший способ дыхания. Если проследить как дышит ребенок, становится заметным, что его передняя брюшная стенка постоянно поднимается и опускается, а грудная клетка остается практически неподвижной. Он “дышит” животом – это так называемый диафрагмальный тип дыхания.
Диафрагма – это мышца, разделяющая грудную и брюшную полости.Сокращения данной мышцы способствуют осуществлению дыхательных движений: вдоха и выдоха.
В повседневной жизни человек не задумывается о дыхании и вспоминает о нем, когда по каким-то причинам становится трудно дышать. Например, в течение жизни напряжение мышц спины, верхнего плечевого пояса, неправильная осанка приводят к тому, что человек начинает “дышать” преимущественно только верхними отделами грудной клетки, при этом объем легких задействуется всего лишь на 20%. Попробуйте положить руку на живот и сделать вдох. Заметили, что рука на животе практически не изменила своего положения, а грудная клетка поднялась. При таком типе дыхания человек задействует преимущественно мышцы грудной клетки (грудной тип дыхания) или области ключиц (ключичное дыхание). Однако как при грудном, так и при ключичном дыхании организм снабжается кислородом в недостаточной степени.
Недостаток поступления кислорода может возникнуть также при изменении ритмичности дыхательных движений, то есть изменении процессов смены вдоха и выдоха.
В состоянии покоя кислород относительно интенсивно поглощается миокардом, серым веществом головного мозга (в частности, корой головного мозга), клетками печени и корковым веществом почек; клетки скелетной мускулатуры, селезенка и белое вещество головного мозга потребляют в состоянии покоя меньший объем кислорода, то при физической нагрузке потребление кислорода миокардом увеличивается в 3-4 раза, а работающими скелетными мышцами – более чем в 20-50 раз по сравнению с покоем.
Интенсивное дыхание, состоящее в увеличении скорости дыхания или его глубины (процесс называется гипервентиляцией), приводит к увеличению поступления кислорода через воздухоносные пути. Однако частая гипервентиляция способна обеднить ткани организма кислородом. Частое и глубокое дыхание приводит к уменьшению количества углекислоты в крови (гипокапнии) и защелачиванию крови – респираторному алкалозу.
Подобный эффект прослеживается, если нетренированный человек осуществляет частые и глубокие дыхательные движения в течение короткого времени. Наблюдаются изменения со стороны как центральной нервной системы (возможно появление головокружения, зевоты, мелькания “мушек” перед глазами и даже потери сознания), так и сердечно-сосудистой системы (появляется одышка, боль в сердце и другие признаки). В основе данных клинических проявлений гипервентиляционного синдрома лежат гипокапнические нарушения, приводящие к уменьшению кровоснабжения головного мозга. В норме у спортсменов в покое после гипервентиляции наступает состояние сна.
Следует отметить, что эффекты, возникающие при гипервентиляции, остаются в то же время физиологичными для организма – ведь на любое физическое и психоэмоциональное напряжение организм человека в первую очередь реагирует изменением характера дыхания.
При глубоком, медленном дыхании (брадипноэ) наблюдается гиповентиляционный эффект. Гиповентиляция – поверхностное и замедленное дыхание, в результате которого в крови отмечается понижение содержание кислорода и резкое увеличение содержания углекислого газа (гиперкапния).
Количество кислорода, которое клетки используют для окислительных процессов, зависит от насыщенности крови кислородом и степени проникновения кислорода из капилляров в ткани.Снижение поступления кислорода приводит к кислородному голоданию и к замедлению окислительных процессов в тканях.
В 1931 году доктор Отто Варбург получил Нобелевскую премию в области медицины, открыв одну из возможных причин возникновения рака. Он установил, что возможной причиной этого заболевания является недостаточный доступ кислорода к клетке.
Используя простые рекомендации, а также различные физические упражнения, можно повысить доступ кислорода к тканям.
- Правильное дыхание, при котором воздух, проходящий через воздухоносные пути, в достаточной степени согревается, увлажняется и очищается – это спокойное, ровное, ритмичное, достаточной глубины.
- Во время ходьбы или выполнения физических упражнений следует не только сохранять ритмичность дыхания, но и правильно сочетать ее с ритмом движения (вдох на 2-3 шага, выдох на 3-4 шага).
- Важно помнить, что потеря ритмичности дыхания приводит к нарушению газообмена в легких, утомлению и развитию других клинических признаков недостатка кислорода.
- При нарушении акта дыхания уменьшается приток крови к тканям и понижается насыщение ее кислородом.
Необходимо помнить, что физические упражнения способствуют укреплению дыхательной мускулатуры и усиливают вентиляцию легких. Таким образом, от правильного дыхания в значительной мере зависит здоровье человека.
Альвеолы. Сурфактант. Поверхностное натяжение слоя жидкости в альвеолах. Закон Лапласа.
Тонкий слой жидкости покрывает поверхность альвеол легких. Переходная граница между воздушной средой и жидкостью имеет поверхностное натяжение, которое формируется межмолекулярными силами и которое будет уменьшать площадь покрываемой молекулами поверхности. Однако миллионы альвеол легких, покрытых мономолекулярным слоем жидкости, не спадаются, поскольку эта жидкость содержит субстанции, которые в целом называются сурфактантом (поверхностно активный агент). Поверхностно активные агенты обладают свойством снижать поверхностное натяжение слоя жидкости в альвеолах легких на границе фаз воздух—жидкость, благодаря которому легкие становятся легко растяжимыми.
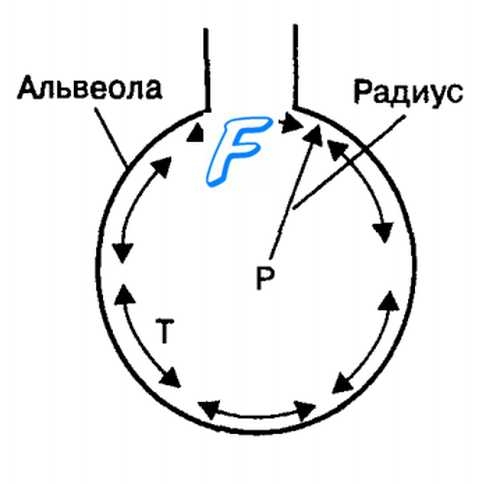
Рис. 10.7. Приложение закона Лапласа к изменению поверхностного натяжения слоя жидкости, покрывающего поверхность альвеол. Изменение радиуса альвеол изменяет в прямой зависимости величину поверхностного натяжения в альвеолах (Т). Давление (Р) внутри альвеол также варьирует при изменении их радиуса: уменьшается при вдохе и увеличивается при выдохе.
Альвеолярный эпителий состоит из плотно контактирующих между собой альвеолоцитов (пневмоцитов) I и II типа и покрыт мономолекулярным слоем сурфактанта, состоящего из фосфолипидов, белков и полисахаридов (глицерофосфолипиды 80 %, глицерол 10 %, белки 10 %). Синтез сурфактанта осуществляется альвеолоцитами II типа из компонентов плазмы крови. Основным компонентом сурфактанта является дипальмитоилфосфатидилхолин (более 50 % фосфолипидов сурфактанта), который адсорбируется на границе фаз жидкость—воздух с помощью белков сурфактанта SP-B и SP-C. Эти белки и глицерофосфолипиды уменьшают поверхностное натяжение слоя жидкости в миллионах альвеол и обеспечивают легочной ткани свойство высокой растяжимости. Поверхностное натяжение слоя жидкости, покрывающей альвеолы, изменяется в прямой зависимости от их радиуса (рис. 10.7). В легких сурфактант изменяет степень поверхностного натяжения поверхностного слоя жидкости в альвеолах при изменении их площади. Это обусловлено тем, что во время дыхательных движений количество сурфактанта в альвеолах остается постоянным. Поэтому при растяжении альвеол во время вдоха слой сурфактанта становится тоньше, что вызывает снижение его действия на поверхностное натяжение в альвеолах. При уменьшении объема альвеол во время выдоха молекулы сурфактанта начинают более плотно прилегать друг к другу и, увеличивая поверхностное давление, снижают поверхностное натяжение на границе фаз воздух—жидкость. Это препятствует спадению (коллапсу) альвеол во время экспирации, независимо от ее глубины. Сурфактант легких влияет на поверхностное натяжение слоя жидкости в альвеолах в зависимости не только от ее площади, но и от направления, в котором происходит изменение площади поверхностного слоя жидкости в альвеолах. Этот эффект сурфактанта называется гистерезисом (рис. 10.8).
Физиологический смысл эффекта заключается в следующем. При вдохе по мере увеличения объема легких под влиянием сурфактанта увеличивается натяжение поверхностного слоя жидкости в альвеолах, что препятствует растяжению легочной ткани и ограничивает глубину инспирации. Напротив, при выдохе поверхностное натяжение жидкости в альвеолах под влиянием сурфактанта уменьшается, но не исчезает полностью. Поэтому даже при самом глубоком выдохе в легких не происходит спадения, т. е. коллапса альвеол.
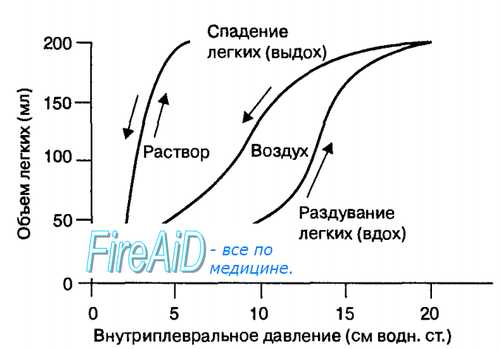
Рис. 10.8. Эффект поверхностного натяжения слоя жидкости на изменение объема легких в зависимости от внутриплеврального давления при раздувании легких солевым раствором и воздухом. Когда объем легких увеличивается за счет их наполнения солевым раствором, то в них отсутствуют поверхностное натяжение и феномен гистерезиса. Относительно интактных легких — площадь петли гистерезиса свидетельствует об увеличении поверхностного натяжения слоя жидкости в альвеолах при вдохе и снижении этой величины при выдохе.
В составе сурфактанта имеются белки типа SP-A и SP-D, благодаря которым сурфактант участвуют в местных иммунных реакциях, опосредуя фагоцитоз, поскольку на мембранах альвеолоцитов II типа и макрофагов имеются рецепторы SP-A. Бактериостатическая активность сурфактанта проявляется в том, что это вещество опсонизирует бактерии, которые затем легче фагоцитируются альвеолярными макрофагами. Кроме того, сурфактант активирует макрофаги и влияет на скорость их миграции в альвеолы из межальвеолярных перегородок. Сурфактант выполняет защитную роль в легких, предотвращая непосредственный контакт альвеолярного эпителия с частицами пыли, агентами инфекционного начала, которые достигают альвеол с вдыхаемым воздухом. Сурфактант способен обволакивать инородные частицы, которые затем транспортируются из респираторной зоны легкого в крупные дыхательные пути и удаляются из них со слизью. Наконец, сурфактант снижает поверхностное натяжение в альвеолах до близких к нулевым величинам и тем самым создает возможность расправления легких при первом вдохе новорожденного.
Поверхность альвеолярного эпителия в лёгких покрыта сурфактантом, необходимым для обеспечения дыхания и адекватной иммунной защиты. Лёгочный сурфактант состоит из липидов (90%) и ряда белков, имеющих различные функции. Сурфактантные белки представлены белками SP-A, SP-D, SP-B и SP-C. В данном обзоре обсуждаются основные функции сурфактантных белков.
Ключевые слова
Обзор
Лёгкие выполняют две главные функции в организме: обеспечение дыхания и функционирование механизмов иммунной защиты. Корректное выполнение данных функций связано с лёгочным сурфактантом.
Сурфактант в лёгких синтезируется альвеолярными клетками II типа и секретируется в альвеолярное пространство. Сурфактант покрывает поверхность альвеолярного эпителия и состоит из липидов (90 %) и белков (10 %), составляя липопротеидный комплекс. Липиды представлены в основном фосфолипидами. Дефицит и/или качественные изменения состава легочного сурфактанта описаны при туберкулезе, респираторном дистресс-синдроме новорожденных, пневмонии и других заболеваниях. 2.
Сурфактантные белки представлены белками SP-A, (Surfactant Protein A, 5,3%), SP-D (0,6 %), SP-B (0,7 %), и SP-C (0,4%). 5.
Функции гидрофильных белков SP-A и SP-D связаны с иммунной защитой в легких. Эти белки связывают липополисахарид грамотрицательных бактерий и агрегируют различные микроорганизмы, влияют на активность тучных, дендритных клеток, лимфоцитов и альвеолярных макрофагов. SP-A ингибирует созревание дендритных клеток, тогда как SP-D увеличивает способность альвеолярных макрофагов к захвату и презентации антигенов, стимулируя адаптивный иммунитет [7,8].
Сурфактантный белок А является наиболее обильным белком лёгочного сурфактанта. Он обладает выраженными иммуномодулирующими свойствами. Белок SP-A воздействует на рост и жизнеспособность микроорганизмов, повышая проницаемость их цитоплазматической мембраны. Более того, SP-A стимулирует хемотаксис макрофагов, влияет на пролиферацию клеток иммунного ответа и на продукцию цитокинов, повышает продукцию реактивных оксидантов, повышает фагоцитоз клеток, подвергшихся апоптозу и стимулирует фагоцитоз бактерий. SP-A человека состоит из двух генных продуктов - SP-A1 и SP-A2, структура и функция которых различна. Наиболее важное различие в структуре SP-A1 и SP-A2- аминокислотная позиция 85 коллагеноподобного региона белка SP-A, где SP-A1 имеет цистеин, а SP-A2 – аргинин. Функциональные различия между SP-A1 и SP-A2 включают их способность стимулировать фагоцитоз, ингибировать секрецию сурфактанта.[7]. Во всех этих случаях SP-A2 обладает большей активностью, чем SP-A1. [8].
Функции гидрофобных белков SP-B и SP-C связаны с обеспечением возможности дыхания. Они снижают поверхностное натяжение в альвеолах и способствуют равномерному распределению сурфактанта на поверхности альвеол. [9].
Механизмы врождённого компонента иммунитета играют важную роль в первичном ответе на инфекцию. Врождённый иммунитет лёгких связан с функцией лёгочного сурфактанта, который наряду с поддержанием необходимого для дыхания поверхностного натяжения, обеспечивает иммунную защиту лёгких. В организме человека белок SP-A (SP-A, Surfactant Protein A), наиболее обильный белок сурфактанта лёгких человека с выраженными иммуномодулирующими свойствами, кодируется двумя генами – SP-A1 и SP-A2. Соотношение белков SP-A1 и SP-A2 в лёгких может отличаться у разных индивидумов. В данном обзоре рассматриваются вопросы, связанные с ролью лёгочного сурфактанта в имунной защите. Описаны строение и функции сурфактантного белка А. Значительное внимание уделено различиям в иммунобиологической активности между SP-A1 и SP-A2 вариантами белка SP-A и механизмам, лежащим в основе данных различий.

1. Surfactant protein A inhibits T cell proliferation via its collagen-like tail and a 210-kDa receptor / P. Borron, F.X. McCormack, B.M. Elhalwagi, Z.C. Chroneos, J.F. Lewis, S. Zhu, J.R. Wright, V.L. Shepherd, F. Possmayer, K. Inchley, L.J. Fraher // Am J Physiol Lung Cell Mol Physiol 275: L679-686. - 1998.
2. Surfactant-associated protein A inhibits LPS-induced cytokine and nitric oxide production in vivo / P. Borron, J.C. McIntosh, T.R. Korfhagen, J.A. Whitsett, J. Taylor, J.R. Wright // Am J Physiol Lung Cell Mol Physiol 278: L840-847. - 2000.
3. Brinker K.G., Garner H., Wright J.R. Surfactant protein A modulates the differentiation of murine bone marrow-derived dendritic cells // Am J Physiol Lung Cell Mol Physiol 284:
4. Chroneos Z.C., Sever-Chroneos Z., Shepherd V.L. Pulmonary surfactant: an immunological perspective // Cell Physiol Biochem 25: 13-26. - 2010.
5. Structural analysis and lipid-binding properties of recombinant human surfactant protein a derived from one or both genes / I. Garcia-Verdugo, G. Wang, J. Floros, C. Casals // Biochemistry 41: 14041-14053. - 2002.
6. By binding SIRPalpha or calreticulin/CD91, lung collectins act as dual function surveillance molecules to suppress or enhance inflammation / S.J. Gardai, Y.Q. Xiao, M. Dickinson, J.A. Nick, D.R. Voelker, K.E. Greene, P.M. Henson // Cell 115: 13-23. - 2003.
7. Pulmonary surfactant, lung function, and endobronchial inflammation in cystic fibrosis / M. Griese, R. Essl, R. Schmidt, E. Rietschel, F. Ratjen, M. Ballmann, K. Paul // Am J Respir Crit Care Med 170: 1000-1005. - 2004.
8. Role of surfactant protein-A in nitric oxide production and mycoplasma killing in congenic C57BL/6 mice / J.M. Hickman-Davis, J. Gibbs-Erwin, J.R. Lindsey, S. Matalon // American journal of respiratory cell and molecular biology 30: 319-325. - 2004.
9. Killing of Klebsiella pneumoniae by human alveolar macrophages / J.M. Hickman-Davis, P. O´Reilly, I.C. Davis, J. Peti-Peterdi, G. Davis, K.R. Young, R.B. Devlin, S. Matalon // Am J Physiol Lung Cell Mol Physiol 282: L944-956. - 2002.
10. Decreased contents of surfactant proteins A and D in BAL fluids of healthy smokers / Y. Honda, H. Takahashi, Y. Kuroki, T. Akino, S. Abe // Chest 109: 1006-1009. - 1996.
11. Hoover R.R., Floros J. Organization of the human SP-A and SP-D loci at 10q22-q23. Physical and radiation hybrid mapping reveal gene order and orientation // American journal of respiratory cell and molecular biology 18: 353-362. - 1998.
12. Surfactant proteins SP-A and SP-D: structure, function and receptors / U. Kishore, T.J. Greenhough, P. Waters, A.K. Shrive, R. Ghai, M.F. Kamran, A.L. Bernal, K.B. Reid, T. Madan, T. Chakraborty // Mol Immunol 43: 1293-1315. - 2006.
13. Kremlev S.G., Phelps D.S. Surfactant protein A stimulation of inflammatory cytokine and immunoglobulin production // Am J Physiol Lung Cell Mol Physiol 267: L712-719. - 1994.
14. Kremlev S.G., Umstead T.M., Phelps D.S. Effects of surfactant protein A and surfactant lipids on lymphocyte proliferation in vitro // Am J Physiol Lung Cell Mol Physiol 267: L357-364. - 1994.
15. Surfactant protein A-deficient mice are susceptible to group B streptococcal infection / A.M. LeVine, M.D. Bruno, K.M. Huelsman, G.F. Ross, J.A. Whitsett, T.R. Korfhagen // J Immunol 158: 4336-4340. - 1997.
16. Surfactant protein-A-deficient mice are susceptible to Pseudomonas aeruginosa infection / A.M. LeVine, K.E. Kurak, M.D. Bruno, J.M. Stark, J.A. Whitsett, T.R. Korfhagen // American journal of respiratory cell and molecular biology 19: 700-708. - 1998.
17. Distinct effects of surfactant protein A or D deficiency during bacterial infection on the lung / A.M. LeVine, J.A. Whitsett, J.A. Gwozdz, T.R. Richardson, J.H. Fisher, M.S. Burhans, T.R. Korfhagen // J Immunol 165: 3934-3940. - 2000.
18. Immunosuppressed surfactant protein A-deficient mice have increased susceptibility to Pneumocystis carinii infection / M.J. Linke, C.E. Harris, T.R. Korfhagen, F.X. McCormack, A.D. Ashbaugh, P. Steele, J.A. Whitsett, P.D. Walzer // J Infect Dis 183: 943-952. - 2001.
19. Surfactant proteins A and D protect mice against pulmonary hypersensitivity induced by Aspergillus fumigatus antigens and allergens / T. Madan, U. Kishore, M. Singh, P. Strong, H. Clark, E.M. Hussain, K.B. Reid, P.U. Sarma // J Clin Invest 107: 467-475. - 2001.
21. SP-A1 and SP-A2 variants differentially enhance association of Pseudomonas aeruginosa with rat alveolar macrophages / A.N. Mikerov, T.M. Umstead, W. Huang, W. Liu, D.S. Phelps, J. Floros // Am J Physiol Lung Cell Mol Physiol 288: 150-158. - 2005.
22. Surfactant protein A2 (SP-A2) variants expressed in CHO cells stimulate phagocytosis of Pseudomonas aeruginosa more than Do SP-A1 variants / A.N. Mikerov, G. Wang, T.M. Umstead, M. Zacharatos, N.J. Thomas, D.S. Phelps, J. Floros // Infect Immun 75: 1403-1412. - 2007.
23. Oberley R.E., Snyder J.M. Recombinant human SP-A1 and SP-A2 proteins have different carbohydrate-binding characteristics //Am J Physiol Lung Cell Mol Physiol 284: L871-881, 2003.
24. Pastva A.M., Wright J.R., Williams K.L. Immuno- modulatory roles of surfactant proteins A and D: implications in lung disease // Proc Am Thorac Soc 4: 252-257. - 2007.
25. Phelps D.S. Surfactant regulation of host defense function in the lung: a question of balance // Pediatr Pathol Mol Med 20: 269-292. - 2001.
26. Schagat T.L., Wofford J.A., Wright J.R. Surfactant protein A enhances alveolar macrophage phagocytosis of apoptotic neutrophils // J Immunol 166: 2727-2733. - 2001.
27. Characterization of a human surfactant protein A1 (SP-A1) gene-specific antibody; SP-A1 content variation among individuals of varying age and pulmonary health / H.R. Tagaram, G. Wang, T.M. Umstead, A.N. Mikerov, N.J. Thomas, G.R. Graff, J.C. Hess, M.J. Thomassen, M.S. Kavuru, D.S. Phelps, J. Floros // American journal of physiology 292: L1052-1063. - 2007.
28. Pulmonary surfactant protein A enhances the host-defense mechanism of rat alveolar macrophages / F. van Iwaar- den, B. Welmers, J. Verhoef, H.P. Haagsman, L.M. van Golde // American journal of respiratory cell and molecular biology 2: 91-98. - 1990.
30. Differences in biochemical properties and in biological function between human SP-A1 and SP-A2 variants, and the impact of ozone-induced oxidation / G. Wang, S.R. Bates-Kenney, J.Q. Tao, D.S. Phelps, J. Floros // Biochemistry 43: 4227-4239. - 2004.
31. Effect of cysteine 85 on biochemical properties and biological function of human surfactant protein A variants Wang G., Myers C., Mikerov A., Floros J. // Biochemistry 46: 8425-8435. - 2007.
32. Wang G., Phelps D.S., Umstead T.M., Floros J. Human SP-A protein variants derived from one or both genes stimulate TNF-alpha production in the THP-1 cell line // Am J Physiol Lung Cell Mol Physiol 278: L946-954. - 2000.
35. Surfactant proteins A and D inhibit the growth of Gram-negative bacteria by increasing membrane permeability / H. Wu, A. Kuzmenko, S. Wan, L. Schaffer, A. Weiss, J.H. Fisher, K.S. Kim, F.X. McCormack // J Clin Invest 111: 1589-1602. - 2003.
36. Розенберг О.А. Лёгочный сурфактант и его применение при заболеваниях лёгких. Общая реаниматология. - 20073. - №1. - С. 66-77.
Известно, что лёгкие выполняют две главные функции в организме: обеспечение дыхания и функционирование механизмов врождённого иммунитета. Для выполнения этих двух функций важное значение отводится лёгочному сурфактанту, покрывающему поверхность альвеолярного эпителия лёгких. Лёгочный сурфактант состоит из липидов (~90 %) и белков (~10 %), представляя собой липопротеидный комплекс. Сурфактантные белки представлены белками SP-A, (Surfactant Protein A, ~5,3 %), SP-D (~0,6 %), SP-B (~0,7 %), and SP-C (~0,4 %). [4]. Компоненты липидной фракции и гидрофобные белки SP-B и SP-C участвуют в снижении поверхностного натяжения в лёгких, что позволяет предотвращать слипание альвеол в конце выдоха. Гидрофильные белки SP-A и SP-D отвечают за регулирование механизмов врождённого иммунитета. Нарушение состава и свойств сурфактанта связано с такими заболеваниями, как респираторный дистресс-синдром новорожденных, острый респираторный дистресс-синдром взрослых, бронхиальная астма, пневмония, туберкулез легких и др. [36].
Сурфактантный белок А (SP-A, Surfactant Protein A) является основным белком лёгочного сурфактанта, обладающим выраженными иммуномодулирующими свойствами. Белок SP-A функционирует как в качестве опсонизирующего агента, так и в качестве иммуномодулятора. Опсонизация и аггрегация патогенных микроорганизмов белком SP-A способствует их последующему фагоцитозу и киллингу. Было показано, что SP-A воздействует на рост и жизнеспособность микроорганизмов, повышая проницаемость микробной клеточной мембраны [35]. Более того, SP-A регулирует механизмы иммунной защиты в лёгких путём связывания звеньев врождённого и приобретённого компонентов иммунитета [3]. Среди регуляторных функций SP-A - его способность стимулировать хемотаксис макрофагов [34], влиять на пролиферацию клеток иммунного ответа [14] и на продукцию провоспалительных цитокинов [2, 13], повышать продукцию реактивных оксидантов [28], регулировать продукцию оксида азота [8], повышать фагоцитоз клеток, подвергшихся апоптозу [26], и стимулировать фагоцитоз [9, 21]. Роль SP-A во многих процессах была также доказана при использовании генетически модифицированных SP-A (-/-) нокаут мышей, у которых отсутсвует ген SP-A. Такие мыши проявляли повышенную чувствительность к ряду патогенных микроорганизмов, включая группу B Streptococcus (GBS) [15], Pseudomonas aeruginosa [16], Haemophillus influenza [17], Pneumocystis carinii [18], Klebsiella pneumonia [20].
Кроме описанных выше функций, SP-A опосредует механизмы аллергических реакций в лёгких, участвуя в удалении аллергена, ингибировании связывания IgE и аллергена и освобождения гистамина, супрессии активации сенсибилизированных базофиллов, тучных клеток или эозинофиллов, супрессии пролиферации В- и Т-клеток, и модуляции иммунного ответа дендритными клетками и макрофагами [12]. В модели на мышах выявлено, что внутриносовое введение SP-A снижает эозинофилию в случае аллергического бронхолёгочного аспергиллёза [19].
Функциональные различия между SP-A1 и SP-A2 включают их способность стимулировать фагоцитоз [21, 22], ингибировать секрецию сурфактанта [30], стимулировать продукцию TNF-a [32], так же, как и различия в их аггрегации и олигомеризации [5, 30]. Во всех этих случаях SP-A2 обладал большей активностью, чем SP-A1. Более того, SP-A2 в большей степени, чем SP-A1, связывал углеводы [23]. Всё это указывает на то, что структурные особенности SP-A2 в большей степени, чем SP-A1, способствуют связыванию с углеводами.
Наиболее важное различие в структуре SP-A1 и SP-A2 - аминокислотная позиция 85 коллагеноподобного региона белка SP-A, где SP-A1 имеет цистеин, а SP-A2 - аргинин. Дополнительный цистеин в SP-A1 может быть вовлечён в формирование межтримерной или внутритримерной дисульфидной связи и может отвечать за различия в олигомеризации SP-A1 и SP-A2 [30]. Было показано, что замена Arg 85 на Cys 85 в SP-A2 приводит к снижению функциональной активности SP-A2 до уровня SP-A1, а замена Cys 85 на Arg 85 в SP-A1 повышает активность SP-A1 до уровня SP-A2. Таким образом, структурные различия в коллагеноподобном домене между SP-A1 и SP-A2 могут отвечать за функциональные различия между ними.
Поскольку продукты гена SP-A2 более функциональны, чем SP-A1, общая активность SP-A в лёгких может зависеть не только от общего содержания SP-A, но и от соотношения SP-A1 к SP-A2. Известно, что заболевания лёгких сопровождаются изменением как общего содержания белка SP-A в бронхоальвеолярной жидкости у различных индивидуумов [7, 10], так и соотношения SP-A1 и SP-A2 в броноальвеолярном лаваже [27]. Следовательно, нарушения экспрессии генов SP-A1 и SP-A2 могут привести к неадекватному соотношению SP-A вариантов в лёгких, что, в свою очередь, может внести вклад в неэффективное модулирование механизмов иммунной защиты в лёгких и соответственно повлиять на остроту и продолжительность инфекционных заболеваний лёгких.
Фёдорова В.А., д.м.н., зав. отделом зоо- и зооантропонозных инфекций ГНУ Саратовского НИВИ РАСХН, г. Саратов;
Процесс дыхания, поступление кислорода в организм при вдохе и удаление из него углекислого газа и паров воды при выдохе. Строение респираторной системы. Ритмичность и различные типы дыхательного процесса. Регуляция дыхания. Разные способы дыхания.
Для нормального протекания обменных процессов в организме человека и животных в равной мере необходим как постоянный приток кислорода, так и непрерывное удаление углекислого газа, накапливающегося в ходе обмена веществ. Такой процесс называется внешним дыханием.
Дыхание – это совокупность процессов, обеспечивающих потребление организмом кислорода и выделение углекислого газа.
Таким образом, дыхание – одна из важнейших функций регулирования жизнедеятельности человеческого организма. В организме человека функцию дыхания обеспечивает дыхательная (респираторная система).
В дыхательную систему входят легкие и респираторный тракт (дыхательные пути), который, в свою очередь, включает носовые ходы, гортань, трахею, бронхи, мелкие бронхи и альвеолы (смотри рисунок 1.5.3). Бронхи разветвляются, распространяясь по всему объему легких, и напоминают крону дерева. Поэтому часто трахею и бронхи со всеми ответвлениями называют бронхиальным деревом.
Кислород в составе воздуха через носовые ходы, гортань, трахею и бронхи попадает в легкие. Концы самых мелких бронхов заканчиваются множеством тонкостенных легочных пузырьков – альвеол (смотри рисунок 1.5.3).
Альвеолы – это 500 миллионов пузырьков диаметром 0,2 мм, где происходит переход кислородом в кровь, удаление углекислого газа из крови.
Здесь и происходит газообмен. Кислород из легочных пузырьков проникает в кровь, а углекислый газ из крови – в легочные пузырьки (рисунок 1.5.4).
Рисунок 1.5.4. Легочный пузырек. Газообмен в легких
Важнейший механизм газообмена – это диффузия, при которой молекулы перемещаются из области их высокого скопления в область низкого содержания без затраты энергии (пассивный транспорт). Перенос кислорода из окружающей среды к клеткам производится путем транспорта кислорода в альвеолы, далее в кровь. Таким образом, венозная кровь обогащается кислородом и превращается в артериальную. Поэтому состав выдыхаемого воздуха отличается от состава наружного воздуха: в нем содержится меньше кислорода и больше углекислого газа, чем в наружном, и много водяных паров (смотри рисунок 1.5.4). Кислород связывается с гемоглобином, который содержится в эритроцитах, насыщенная кислородом кровь поступает в сердце и выталкивается в большой круг кровообращения. По нему кровь разносит кислород по всем тканям организма. Поступление кислорода в ткани обеспечивает их оптимальное функционирование, при недостаточном же поступлении наблюдается процесс кислородного голодания (гипоксии).
Недостаточное поступление кислорода может быть обусловлено несколькими причинами как внешними (уменьшение содержания кислорода во вдыхаемом воздухе), так и внутренними (состояние организма в данный момент времени). Пониженное содержание кислорода во вдыхаемом воздухе, так же как и увеличение содержания углекислого газа и других вредных токсических веществ наблюдается в связи с ухудшением экологической обстановки и загрязнением атмосферного воздуха. По данным экологов только 15% горожан проживают на территории с допустимым уровнем загрязнения воздуха, в большинстве же районов содержание углекислого газа увеличено в несколько раз.
При очень многих физиологических состояниях организма (подъем в гору, интенсивная мышечная нагрузка), так же как и при различных патологических процессах (заболевания сердечно-сосудистой, дыхательной и других систем) в организме также может наблюдаться гипоксия.
Природа выработала множество способов, с помощью которых организм приспосабливается к различным условиям существования, в том числе к гипоксии. Так компенсаторной реакцией организма, направленной на дополнительное поступление кислорода и скорейшее выведение избыточного количества углекислого газа из организма является углубление и учащение дыхания. Чем глубже дыхание, тем лучше вентилируются легкие и тем больше кислорода поступает к клеткам тканей.
К примеру, во время мышечной работы усиление вентиляции легких обеспечивает возрастающие потребности организма в кислороде. Если в покое глубина дыхания (объем воздуха, вдыхаемого или выдыхаемого за один вдох или выдох) составляет 0,5 л, то во время напряженной мышечной работы она увеличивается до 2-4 л в 1 минуту. Расширяются кровеносные сосуды легких и дыхательных путей (а также дыхательных мышц), увеличивается скорость тока крови по сосудам внутренних органов. Активируется работа дыхательных нейронов. Кроме того, в мышечной ткани есть особый белок (миоглобин), способный обратимо связывать кислород. 1 г миоглобина может связать примерно до 1,34 мл кислорода. Запасы кислорода в сердце составляют около 0,005 мл кислорода на 1 г ткани и этого количества в условиях полного прекращения доставки кислорода к миокарду может хватить для того, чтобы поддерживать окислительные процессы лишь в течение примерно 3-4 с.
Миоглобин играет роль кратковременного депо кислорода. В миокарде кислород, связанный с миоглобином, обеспечивает окислительные процессы в тех участках, кровоснабжение которых на короткий срок нарушается.
В начальном периоде интенсивной мышечной нагрузки увеличенные потребности скелетных мышц в кислороде частично удовлетворяются за счет кислорода, высвобождающегося миоглобином. В дальнейшем возрастает мышечный кровоток, и поступление кислорода к мышцам вновь становится адекватным.
Все эти факторы, включая усиление вентиляции легких, компенсируют кислородный “долг”, который наблюдается при физической работе. Естественно, увеличению доставки кислорода к работающим мышцам и удалению углекислого газа способствует согласованное увеличение кровообращения в других системах организма.
Саморегуляция дыхания. Организм осуществляет тонкое регулирование содержания кислорода и углекислого газа в крови, которое остается относительно постоянным, несмотря на колебания количества поступающего кислорода и потребности в нем. Во всех случаях регуляция интенсивности дыхания направлена на конечный приспособительный результат – оптимизацию газового состава внутренней среды организма.
Частота и глубина дыхания регулируются нервной системой – ее центральными (дыхательный центр) и периферическими (вегетативными) звеньями. В дыхательном центре, расположенном в головном мозге, имеются центр вдоха и центр выдоха.
Дыхательный центр представляет совокупность нейронов, расположенных в продолговатом мозге центральной нервной системы.
При нормальном дыхании центр вдоха посылает ритмические сигналы к мышцам груди и диафрагме, стимулируя их сокращение. Ритмические сигналы образуются в результате спонтанного образования электрических импульсов нейронами дыхательного центра.
Сокращение дыхательных мышц приводит к увеличению объема грудной полости, в результате чего воздух входит в легкие. По мере увеличения объема легких возбуждаются рецепторы растяжения, расположенные в стенках легких; они посылают сигналы в мозг – в центр выдоха. Этот центр подавляет активность центра вдоха, и поток импульсных сигналов к дыхательным мышцам прекращается. Мышцы расслабляются, объем грудной полости уменьшается, и воздух из легких вытесняется наружу (смотри рисунок 1.5.5).
Рисунок 1.5.5. Регуляция дыхания
Процесс дыхания, как уже отмечалось, состоит из легочного (внешнего) дыхания, а также транспорта газа кровью и тканевого (внутреннего) дыхания. Если клетки организма начинают интенсивно использовать кислород и выделять много углекислого газа, то в крови повышается концентрация угольной кислоты. Кроме того, увеличивается содержание молочной кислоты в крови за счет усиленного образования ее в мышцах. Данные кислоты стимулируют дыхательный центр, и частота и глубина дыхания увеличиваются. Это еще один уровень регуляции. В стенках крупных сосудов, отходящих от сердца, имеются специальные рецепторы, реагирующие на понижение уровня кислорода в крови. Эти рецепторы также стимулируют дыхательный центр, повышая интенсивность дыхания. Данный принцип автоматической регуляции дыхания лежит в основе бессознательного управления дыханием, что позволяет сохранить правильную работу всех органов и систем независимо от условий, в которых находится организм человека.
Ритмичность дыхательного процесса, различные типы дыхания. В норме дыхание представлено равномерными дыхательными циклами “вдох – выдох” до 12-16 дыхательных движений в минуту. В среднем такой акт дыхания совершается за 4-6 с. Акт вдоха проходит несколько быстрее, чем акт выдоха (соотношение длительности вдоха и выдоха в норме составляет 1:1,1 или 1:1,4). Такой тип дыхания называется эйпноэ (дословно – хорошее дыхание). При разговоре, приеме пищи ритм дыхания временно меняется: периодически могут наступать задержки дыхания на вдохе или на выходе (апноэ). Во время сна также возможно изменение ритма дыхания: в период медленного сна дыхание становится поверхностным и редким, а в период быстрого – углубляется и учащается. При физической нагрузке за счет повышенной потребности в кислороде возрастает частота и глубина дыхания, и, в зависимости от интенсивности работы, частота дыхательных движений может достигать 40 в минуту.
При смехе, вздохе, кашле, разговоре, пении происходят определенные изменения ритма дыхания по сравнению с так называемым нормальным автоматическим дыханием. Из этого следует, что способ и ритм дыхания можно целенаправленно регулировать с помощью сознательного изменения ритма дыхания.
Человек рождается уже с умением использовать лучший способ дыхания. Если проследить как дышит ребенок, становится заметным, что его передняя брюшная стенка постоянно поднимается и опускается, а грудная клетка остается практически неподвижной. Он “дышит” животом – это так называемый диафрагмальный тип дыхания.
Диафрагма – это мышца, разделяющая грудную и брюшную полости.Сокращения данной мышцы способствуют осуществлению дыхательных движений: вдоха и выдоха.
В повседневной жизни человек не задумывается о дыхании и вспоминает о нем, когда по каким-то причинам становится трудно дышать. Например, в течение жизни напряжение мышц спины, верхнего плечевого пояса, неправильная осанка приводят к тому, что человек начинает “дышать” преимущественно только верхними отделами грудной клетки, при этом объем легких задействуется всего лишь на 20%. Попробуйте положить руку на живот и сделать вдох. Заметили, что рука на животе практически не изменила своего положения, а грудная клетка поднялась. При таком типе дыхания человек задействует преимущественно мышцы грудной клетки (грудной тип дыхания) или области ключиц (ключичное дыхание). Однако как при грудном, так и при ключичном дыхании организм снабжается кислородом в недостаточной степени.
Недостаток поступления кислорода может возникнуть также при изменении ритмичности дыхательных движений, то есть изменении процессов смены вдоха и выдоха.
В состоянии покоя кислород относительно интенсивно поглощается миокардом, серым веществом головного мозга (в частности, корой головного мозга), клетками печени и корковым веществом почек; клетки скелетной мускулатуры, селезенка и белое вещество головного мозга потребляют в состоянии покоя меньший объем кислорода, то при физической нагрузке потребление кислорода миокардом увеличивается в 3-4 раза, а работающими скелетными мышцами – более чем в 20-50 раз по сравнению с покоем.
Интенсивное дыхание, состоящее в увеличении скорости дыхания или его глубины (процесс называется гипервентиляцией), приводит к увеличению поступления кислорода через воздухоносные пути. Однако частая гипервентиляция способна обеднить ткани организма кислородом. Частое и глубокое дыхание приводит к уменьшению количества углекислоты в крови (гипокапнии) и защелачиванию крови – респираторному алкалозу.
Подобный эффект прослеживается, если нетренированный человек осуществляет частые и глубокие дыхательные движения в течение короткого времени. Наблюдаются изменения со стороны как центральной нервной системы (возможно появление головокружения, зевоты, мелькания “мушек” перед глазами и даже потери сознания), так и сердечно-сосудистой системы (появляется одышка, боль в сердце и другие признаки). В основе данных клинических проявлений гипервентиляционного синдрома лежат гипокапнические нарушения, приводящие к уменьшению кровоснабжения головного мозга. В норме у спортсменов в покое после гипервентиляции наступает состояние сна.
Следует отметить, что эффекты, возникающие при гипервентиляции, остаются в то же время физиологичными для организма – ведь на любое физическое и психоэмоциональное напряжение организм человека в первую очередь реагирует изменением характера дыхания.
При глубоком, медленном дыхании (брадипноэ) наблюдается гиповентиляционный эффект. Гиповентиляция – поверхностное и замедленное дыхание, в результате которого в крови отмечается понижение содержание кислорода и резкое увеличение содержания углекислого газа (гиперкапния).
Количество кислорода, которое клетки используют для окислительных процессов, зависит от насыщенности крови кислородом и степени проникновения кислорода из капилляров в ткани.Снижение поступления кислорода приводит к кислородному голоданию и к замедлению окислительных процессов в тканях.
В 1931 году доктор Отто Варбург получил Нобелевскую премию в области медицины, открыв одну из возможных причин возникновения рака. Он установил, что возможной причиной этого заболевания является недостаточный доступ кислорода к клетке.
Используя простые рекомендации, а также различные физические упражнения, можно повысить доступ кислорода к тканям.
- Правильное дыхание, при котором воздух, проходящий через воздухоносные пути, в достаточной степени согревается, увлажняется и очищается – это спокойное, ровное, ритмичное, достаточной глубины.
- Во время ходьбы или выполнения физических упражнений следует не только сохранять ритмичность дыхания, но и правильно сочетать ее с ритмом движения (вдох на 2-3 шага, выдох на 3-4 шага).
- Важно помнить, что потеря ритмичности дыхания приводит к нарушению газообмена в легких, утомлению и развитию других клинических признаков недостатка кислорода.
- При нарушении акта дыхания уменьшается приток крови к тканям и понижается насыщение ее кислородом.
Необходимо помнить, что физические упражнения способствуют укреплению дыхательной мускулатуры и усиливают вентиляцию легких. Таким образом, от правильного дыхания в значительной мере зависит здоровье человека.
Читайте также:

