Вирус черной лагуны доклад
Обновлено: 05.07.2024
Когда-то давно одна из веток в популяции гоминид, все больше отделяясь, стала постепенно обретать морфологию и образ жизни человека нынешнего, – так сказать, разумного. Но история вирусов началась задолго до нашей. Задолго до того, как наш мозг развился к способности задавать вопросы. И задолго до того, как мы стали сначала догадываться, а потом и понимать, – от чего, собственно, болеем и умираем. Сегодня на одной планете с нами живет неисчислимое количество вирусов; по некоторым оценкам, их здесь сформировалось более ста миллионов разновидностей (представляете себе, например, сто миллионов человеческих рас?), и если каким-то чудом пересчитать все вирусы поштучно, то численность этой популяции значительно превзойдет состав всех прочих популяций, вместе взятых, включая даже бактерии и насекомых. Вирусы фантастически разнообразны во всех аспектах своего существования, особенно в размерах, форме и предпочтениях. А мы до сих пор не решили даже, можно ли их считать живыми.
Любое живое существо на Земле, – во всей биомассе от бактерий и простейших до слона и баобаба, – заражается теми или иными вирусами. Некоторые вирусы колонизируют представителей какого-то одного вида, другие не столь привередливы. К человеку абсолютное большинство из них относится нейтрально. Но все они, – внутриклеточные паразиты, которые перестраивают геном зараженной клетки на свой лад, на репликацию все новых и новых своих копий. Активно существовать и размножаться вне живой клетки вирусы не могут. Пассивное же их существование и, вообще, этот странный вирусный мир, где даже гравитация работает как-то не так, нам представить довольно сложно.
В целом, при заражении наша судьба зависит от общего состояния здоровья и актуального иммунного статуса, от инфицирующей дозы (численность попавшей в организм колонии) и поведения самого вируса. Клетки-то не просто инфицируются; какое-то время они работают как фабрика вирусов, а при разрушении мембраны неизбежно погибают, и если это происходит в массовом порядке, да в жизненно важном органе, который не восстанавливается…
Для Homo sapiens’а, который привык считать себя центром мироздания и венцом творения, Великая вирусная война как-то… оскорбительна, что ли. Действительно, в ней ведь нет ничего личного. Вообще ничего. Враг попросту не знает о том, что он – враг, что существуем такие себе высокоразвитые мы, что нам не нравится болеть и умирать. Когда на человека нападал опасный хищник-людоед (например, другой Homo sapiens), это всегда была какая-то схватка, какая-то ярость, хоть какие-то шансы. А этого врага даже не увидишь в лицо, потому что лица у него нет. Ему нечем и незачем нас ненавидеть, нечем о нас знать и думать, нечем испытывать к нам аппетит. Его и самого-то, врага этого, практически нет, настолько он мал. Наш организм для него – нечто вроде Галактики, с которой из-за разности в масштабах невозможно пребывать в каких-то личных отношениях. Мы – просто мир обитания, место и способ существования. Вот они и существуют в своем измерении, пока им существуется. Кстати говоря: когда мы своими бензопилами, заводами и фабриками, потребностями и отходами уничтожаем породившую нас природу, – мы ведь делаем это не потому, что мы плохие, ненавидим свою планету и целенаправленно торопимся довести ее до нежилого состояния. Вовсе нет. Просто вот такой у нас получается course of events, как сказал бы англичанин. Такой ход событий, курс нашего (паразитического, выходит?!) развития. И, кстати, не случайно мы в последние годы все чаще сравниваем с вирусами самих себя, – в пересчете на масштабы, конечно. Сравнив, неприятно удивляемся: а и правда, много ведь общего. Только мы, пожалуй, поагрессивней будем, подеструктивней, покатастрофичней для своей экосистемы в целом. И природа, возможно, пытается сдерживать нас с помощью мелких и мельчайших, – есть и такая теория. Именно сдерживать. Если бы от нас по-настоящему хотели избавиться, уже давно избавились бы, так что полное вымирание нам, видимо, не грозит, – во всяком случае, вымирание от инфекционных болезней. Это по отдельности мы теперь стали нежны и уязвимы, а как вид мы остаемся очень цепкими, живучими, плодовитыми и настырными. Даже теряя сотни миллионов, быстро восстанавливаемся в миллиардах. К тому же известно, что ни один паразит не заинтересован в том, чтобы уничтожить своих хозяев как вид, вывести его вчистую. Даже если этот вид опасен для всех.
А кто из них по-настоящему опасен для нас?
Вакцины уже есть, но никаких ощутимых результатов пока нет, да и вообще не очень понятно, как там у нас обстоят дела с иммунитетом к коронавирусу.
В целом, пока совсем не похоже, что пандемия идет (или пойдет в ближайшем будущем) на спад. Более вероятным представляется дальнейшее развитие.
Учитывая все вышесказанное, наверное, лучше бы нам понимать, с чем мы имеем дело.
Далее – о двенадцати самых опасных для человека вирусах (по версии экспертов ресурса Live Science).
Марбургский вирус
Вирус Эбола
Широко известный вирус, вызывающий геморрагическую лихорадку. Ее клинические проявления и пути распространения в целом подобны описанным выше; сам вирус также имеет генетическую структуру, аналогичную Марбургскому вирусу, однако представляет собой отдельный серотип (т.е. вызывает несколько отличный иммунный отклик). По состоянию на 2018 год было известно шесть видов эболавируса, каждый из которых имеет собственную специфику. Наиболее опасным является заирский штамм; эпоним Эбола – название реки в Заире (ныне Демократическая республика Конго), где этот вид впервые был идентифицирован.
Вирус бешенства
Вирус иммунодефицита человека
Заболевание, известное сегодня во всем мире как AIDS (СПИД, синдром приобретенного иммунодефицита), появилось и стало объектом исследований с начала 1980 годов, – сначала на выборках гомосексуалистов и инъекционных наркоманов, затем в других категориях населения (в частности, у пациентов, получавших переливание препаратов крови). Инфекционная этиология предполагалась с самого начала; в 1985 году возбудитель был выделен и идентифицирован как ВИЧ, вирус иммунодефицита человека. ВИЧ относится к семейству ретровирусов, отличается продолжительным инкубационным периодом и, как следует из названия, приводит к постепенному ослаблению иммунной системы. СПИД – это терминальная стадия ВИЧ-инфекции, когда организм становится абсолютно беззащитным перед любыми, в том числе условными патогенами, – как внешними, так и внутренними (например, раковыми клетками).
Современные молекулярно-генетические исследования свидетельствуют о том, что правирус иммунодефицита появился в животном мире Африки сто с небольшим лет назад, и, неоднократно мутировав, за несколько десятилетий эволюции обрел способность инфицировать и вызывать заболевание у человека. Быстрому распространению вируса сначала в африканских странах, а затем и по всему миру, способствовал ряд социально-экономических факторов. По оценкам ВОЗ, с момента идентификации ВИЧ-СПИД различные типы и подтипы вируса унесли жизни более чем 32 миллионов человек, что является наибольшими потерями от инфекционных болезней на современном этапе. До 95% новых случаев заражения приходится на беднейшие страны; более двух третей всех инфицированных проживает в Африканском регионе ВОЗ (каждый двадцать пятый взрослый там является, как минимум, носителем).
Вирус оспы
Вирус характеризуется… вернее, характеризовался, поскольку натуральная оспа теперь уже относится к побежденным болезням: естественного вируса оспы в природе не существует. Он характеризовался очень высокой контагиозностью (заразностью), вирулентностью (способностью вызывать заболевание у носителя) и летальностью, – что в совокупности делало оспу одной из опаснейших инфекционных болезней в истории человечества. Эволюция вируса Variola насчитывает десятки тысяч лет, но способность инфицировать человека, как считают современные исследователи, у вируса развилась не ранее, чем две тысячи лет назад; произошло это, видимо, на Ближнем Востоке или в Северной Африке. В начале нашей эры от эпидемий черной оспы страдала, прежде всего, Европа и Азия (Китай, Корея, Индия, Япония), где у выживших вырабатывался устойчивый иммунитет. В тех регионах, куда вирус был занесен позднее, эпидемии носили катастрофический характер: например, 90% коренного населения Америки было уничтожено не мушкетами и винчестерами, а вирусом оспы, и затем уже другими инфекциями, вирусными и бактериальными.
Оспа побеждена, теперь это лишь история, и мы очень надеемся, что никто и никогда из землян уже не будет инфицирован этим вирусом.
Тем не менее, продолжаются работы по созданию противооспенных вакцин; совсем недавно появился даже этиотропный препарат. Уместно повторить: никогда и ни в чем нельзя быть уверенным до конца (даже в высшей защите, которая была и в Ухане), если речь идет о вирусах. К сожалению, есть все основания опасаться, – особенно в нашем неспокойном мире с его терроризмом и ползучими идеями о биологическом оружии. Попади вирус оспы в беспечные, алчные или, хуже того, в недобрые руки (особенно если эти руки окажутся еще и умелыми по части генетической модификации) – и последствия будут… в общем, лучше не думать. С другой стороны, а как об этом не думать, если в 2014 году в одном из американских Национальных институтов здоровья кто-то из сотрудников в очередной раз открыл никем не охраняемый лабораторный холодильник, вдруг заинтересовался давно и невостребованно стоящей пробиркой, вынул ее (слава богу, со всеми необходимыми предосторожностями) – и вот, пожалуйста: пробирочка с черной оспой, забытая, как потом оказалось, еще в 50-е годы. А этот вирус, в отличие от многих других, очень устойчив, и за все шестьдесят лет он так и не утратил жизнеспособность.
Этот образец уничтожен. Но действительно ли он был последним?
Хантавирус
Вирус изолирован и описан Хо Вангом Ли в 1976 году. В дальнейшем было выделено множество разновидностей хантавируса, которые условно можно разделить на две крупные группы – евразийскую и американскую.
Первая группа, широко распространенная в Азии и Европе (в том числе в 61 субъекте Российской Федерации по обе стороны от Урала), при инфицировании человека вызывает ГЛПС, геморрагическую лихорадку с почечным синдромом. Это наиболее частая из всех острых природно-очаговых инфекций. Протекает с высокой температурой, кровотечениями, серьезным поражением почек и рядом тяжелых сопутствующих дисфункций в различных системах организма. Летальность выше в азиатских регионах (до 10-12%).
Все хантавирусы переносятся грызунами и, реже, рукокрылыми. Человек инфицируется при вдыхании, попадании с пищей или при прямом контакте с продуктами жизнедеятельности либо иным биоматериалом зараженного грызуна. Передача от человека к человеку зафиксирована лишь в единичных случаях в Южной Америке.
Этиотропные средства на данном этапе находятся в стадии разработки, вакцины – в стадии клинических испытаний и внедрения. Лечение на сегодняшний день всегда паллиативное, сугубо симптоматическое. Эпидемиологические данные по хантавирусным инфекциям постоянно отслеживаются и уточняются соответствующими службами.
Вирус гриппа
Но даже в те годы, когда сезонная эпидемия гриппа вызывается не самым агрессивным штаммом, она протекает тяжело у нескольких миллионов человек и уносит от 300 до 500 тысяч жизней. Это при летальности менее одного процента для гриппа А. Грипп В более смертоносен, но он реже приобретает размах эпидемий и пандемий.
Первые упоминания или описания похожих на грипп болезней, явно инфекционных и явно респираторных, встречаются еще до нашей эры, – у Гиппократа, например. Первым достоверным описанием пандемии принято считать источник ХVI века.
Клиническая картина неспецифична и, в принципе, одинакова для всех ОРВИ. Точный диагноз может быть установлен только лабораторно, с помощью серологического анализа или полимеразной цепной реакции, однако в абсолютном большинстве случаев сезонный грипп диагностируют клинически, с учетом актуальной эпидемиологической обстановки в регионе.
Заболевание разрешается в течение 7-10 дней и, как правило, не требует госпитализации. Лечение до сих пор было сугубо паллиативным и/или косвенным, иммуностимулирующим, хотя в последние годы сообщалось о создании нескольких эффективных этиотропных противогриппозных препаратов.
Основное средство профилактики и сдерживания эпидемий гриппа – вакцинация, поскольку иммунитет является стойким и достаточно надежным. Основной путь передачи инфекции, как и у всех ОРВИ, – воздушно-капельный.
Однако грипп – это все-таки вирусная инфекция, а вирусы, повторим вновь и вновь, опасны своей непредсказуемостью и своими осложнениями.
К гриппу это относится, пожалуй, в самой полной мере. Вирусы Influenzaviridae, особенно тип А, чрезвычайно изменчивы, они постоянно ищут и находят способы обходить иммунитет (в том числе созданный вакциной для прошлогодних штаммов), поэтому нередко мутации оказываются весьма опасными.
Что касается осложнений, то наиболее тяжелые из них развиваются со стороны легких, печени, сердца, периферической и центральной нервной системы. Наибольшая летальность наблюдается в самой младшей и самой старшей возрастных категориях, когда иммунная система либо еще недостаточно сформирована, либо уже ослаблена.
Вирус денге
Вирус денге может колонизировать организм приматов (включая человека) и летучих мышей, а главным фактором трансмиссии служат кровососущие комары Aedes, выступающие также переносчиками многих других инфекционных заболеваний. Поэтому в эндемичных по денге странах борьба с размножением комаров является одной из важнейших государственных задач.
Тяжелый вариант денге протекает в форме геморрагической лихорадки, чаще встречается у многократно инфицированных жителей регионов, наиболее неблагополучных в эпидемиологическом плане.
Летальность при типичной форме лихорадки денге – порядка 2-2.5%, но геморрагическая форма убивает до половины заболевших. Ежегодная заболеваемость составляет 50-500 миллионов новых случаев, до полумиллиона больных госпитализируются и до 20000 человек умирают. Столь высокие показатели обусловлены тем, что в эндемичной зоне земного шара проживает примерно 40% человечества, и в последние годы специалисты ВОЗ с тревогой говорят о том, что по мере глобального потепления это опасное заболевание неизбежно будет подниматься на север. Разработанные к настоящему времени вакцины рекомендуется применять лишь у ранее уже инфицированных и переболевших; иммунная защита вырабатывается лишь к одному типу лихорадки, тогда как к другим серотипам человек остается восприимчивым, – и это главная проблема в аспекте иммунизации. Лечение симптоматическое, этиопатогенетической терапии пока не существует.
Ротавирус
Лечение симптоматическое, основной задачей выступает регидратация и дезинтоксикация. Доступны вакцины. Этиотропных препаратов пока нет.
В эпидемиологическом плане ротавирусные инфекции являются глобальной проблемой: они широко распространены по всему миру. Заболеваемость оценивается на уровне 25 миллионов новых случаев в год, летальность составляет порядка 3% с большим разбросом, – от 600 до 900 тысяч человек ежегодно умирают, из них до полумиллиона – дети в возрасте до пяти лет. Тяжелые формы течения с летальным исходом регистрируются, в основном, в регионах со слаборазвитой медициной, однако встречаются и в развитых странах, т.е. опасность ротавирусов не следует недооценивать в любом случае.
Вирус SARS-CoV
Судя по заголовкам пунктов, статья становится всё актуальнее, не так ли?
Вирус MERS-CoV
Вспышка началась осенью 2012 году в Саудовской Аравии, затем охватила соседние страны; весной 2015 года бетакоронавирус (родовое название) был завезен в Южную Корею, где уже к осени очаг, – а это была самая серьезная вспышка за пределами Ближнего Востока, – удалось локализовать и подавить.
Бетакоронавирусный респираторный синдром характеризуется тяжелым течением, выраженной лихорадкой, кашлем, затруднениями дыхания и общей гипоксией; в случаях развития тяжелой вирусной пневмонии наблюдается прогрессирующая дыхательная и, нередко, почечная недостаточность, – что и приводит к летальным исходам.
Вирус SARS-CoV-2
Ну вот и добрались. В своих публикациях мы обещали обсудить самые наболевшие вопросы, связанные с продолжающейся в настоящее время пандемией коронавирусной болезни CoViD-19 (это официальное и единственно корректное международное наименование). Ситуацию с этим заболеванием мы отслеживаем и освещаем в новостной ленте чуть ли не с самого начала, и мы готовы говорить об этом.
Обратите внимание на редакторский комментарий к ней, датированный мартом 2020 года. Его мы переведем полностью:
Мы не знаем. В штате Лахта Клиники пока, к сожалению, нет высококвалифицированных специалистов в области молекулярной генетики. И было бы верхом безответственности занимать какую бы то ни было позицию и поддерживать какое бы то ни было мнение, не имея на то достаточной информации (вполне возможно, она и впрямь когда-нибудь всплывет) и достаточной компетентности.
Сейчас вообще не это главное.
Пора, кажется, действовать осмотрительно, умно, информированно и, главное, коллективно.
Мы сейчас на осадном положении. Мы все сейчас в одной лодке, – понимаете? – весь земной шар, все человечество.
Bunyaviridae содержит род Hantavirus, который состоит по крайней мере из 4 серологических групп с 9 вирусами, вызывающими 2 основных, иногда перекрывающих друг друга клинических синдрома:
Вирусами, вызывающими геморрагическую лихорадку с почечным синдромом, являются Хантаан, Сеул, Добрава (Белград) и Пуумала. Вирусы, вызывающие ХЛС в Северной Америке: Sin Nombre, Black Creek Canal, Bayou; в Панаме – Choclo; в Аргентине, Чили, восточной Боливии – Andes ; в Боливии – Leguna Negra (1 Общие справочные материалы Bunyaviridae содержит род Hantavirus, который состоит по крайней мере из 4 серологических групп с 9 вирусами, вызывающими 2 основных, иногда перекрывающих друг друга клинических синдрома: Геморрагическая. Прочитайте дополнительные сведения ).
Хантавирусы выявляются по всему миру у диких грызунов, которые распространяют вирус в течение всей своей жизни через мочу и экскременты. Передача происходит между грызунами. Передача инфекции к человеку происходит через вдыхание пыли, содержащей частицы экскрементов грызунов или через их укусы (редко). Последние данные свидетельствуют о том, что от человека к человеку может возникать передача вируса Андес. Инфекции, приобретаемые естественным образом и в лаборатории, регистрируются всё чаще.
Лабораторный диагноз хантавирусной инфекции устанавливается с помощью серологических тестов и полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). Серологические анализы включают иммуноферментный анализ (ИФА) и Вестерн-блоттинг, а также стрип-блоттинг. Серологическая диагностика в Северной Америке должна быть способной дифференцировать инфекции, вызванные вирусами Сеул (Seoul) и Син Номбре (Sin Nombre) из-за потенциальной перекрестной реактивности. Культивирование вируса является технически трудным, и требуется лаборатория с 3 уровнем биологической безопасности.
Общие справочные материалы
1. Milholland MT, Castro-Arellano I, Suzán G, et al: Global diversity and distribution of hantaviruses and their hosts. EcoHealth 15 (1):163-208, 2018. doi:10.1007/s10393-017-1305-2.
Геморрагическая лихорадка с почечным синдромом
Геморрагическая лихорадка с почечным синдромом начинается как похожее на грипп заболевание и может прогрессировать до шока, кровотечения и почечной недостаточности. Диагноз ставится с помощью серологического анализа и полимеразной цепной реакции (ПЦР). Смертность составляет 6–15%. Лечение включает рибавирин внутривенно.
Некоторые формы геморрагической лихорадки с почечным синдромом имеют легкую форму (например, эпидемическая нефропатия, вызываемая вирусом Пуумала, которая встречается в Скандинавии, западной части бывшего Советского Союза и Европе). Некоторые из них, как правило, протекают легко, но иногда течение болезни может быть тяжелым (например, вирус Сеул, который имеет повсеместное распространение у диких бурых и домашних крыс). Другие формы лихорадки – тяжелые (например, вызванные вирусом Хантаан, как это происходит в Корее, Китае и России, или вирусом Добрава, как это происходит на Балканах).
Инфекция передается людям при вдыхании пыли, инфицированной выделениями грызунов.
Клинические проявления
Инкубация – приблизительно 2 недели.
При легких формах инфекция часто бессимптомна.
При манифестных формах ГЛПС начало заболевания внезапное, с высокой температурой тела, головной болью, болью в спине и животе.
Характерна относительная брадикардия, преходящая умеренная гипотония наблюдается приблизительно у половины пациентов, шок – реже. После 4-го дня развивается почечная недостаточность.
У приблизительно 20% пациентов наблюдается притупление чувствительности. Припадки или тяжелые фокальные неврологические симптомы проявляются у 1%. Сыпь исчезает; у пациентов развивается полиурия, и они выздоравливают через несколько недель. Протеинурия, гематурия и пиурия также могут наблюдаться; возможно возникновение почечной недостаточности.
Диагностика
Серологический анализ или полимеразная цепная реакция (ПЦР)
Геморрагическая лихорадка с почечным синдромом может быть заподозрена у пациентов с возможным заражением вирусом, если у них есть лихорадка, склонность к кровоизлияниям и кровотечениям и почечная недостаточность.
В таких случаях проводят общий анализ крови, тест уровня электролита, анализы функции почек, анализы коагуляции и анализ мочи. Во время гипотензивной фазы продолжается увеличение гематокритного числа и лейкоцитоза и развивается тромбоцитопения. Альбуминурия, гематурия и выбросы красных и белых кровяных телец могут наблюдаться обычно между 2 и 5 днями. Во время полиурической фазы часто наблюдаются отклонения в электролитном составе крови.
Диагноз геморрагической лихорадки с почечным синдромом в конечном счете основывается на серологическом анализе или ПЦР.
Прогноз
Смерть может наступить во время полиурической фазы вследствие нарушений водно-электролитного баланса или вторичных инфекций. Восстановление обычно занимает 3–6 недель, но может понадобиться до 6 месяцев.
В целом летальность составляет 6–15%, как правило, у пациентов с более тяжелыми формами. Остаточная почечная дисфункция нехарактерна, кроме случаев болезни в тяжелой форме, которая выявляется на Балканах.
Лечение
Лечение геморрагической лихорадки с почечным синдромом проводится рибавирином внутривенно: ударная доза 33 мг/кг (максимум 2,64 г), затем 16 мг/кг каждые 6 часов (максимум 1,28 г каждые 6 часов) в течение 4 дней, затем 8 мг/кг каждые 8 часов (максимум 0,64 г каждые 8 часов) в течение 3 дней.
Поддерживающий уход, который может включать гемодиализ, важен, особенно во время полиурической фазы.
Хантавирусный легочный синдром
Хантавирусный легочный синдром (ХТС) регистрируется в США (главным образом, в юго-западных штатах), Канаде (главным образом, в западных провинциях) и в Южной Америке и Панаме. Начинается как грипп и в течение нескольких дней вызывает некардиогенный легочный отек. Диагноз ставится с помощью серологического анализа и полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). При более тяжелых случаях заболевания смертность достигает 50%. Лечение носит поддерживающий характер.
Большинство случаев ХЛС вызваны
Хантавирусом Син Номбре (вирус "Четыре угла", вирус Каньона Муэрто), вирусом Анд и хантавирусом Choclo
Вирусами Black Creek Canal, Muleshoe или вирусом Bayou в юго-восточной части США и в Мексике
Вирусом New York (вариантом вируса Sin Nombre) на Восточном побережье США
Хантавирусы Convict Creek и Isla Vista распространены на территории западного побережья Северной Америки
Вирусы Черной лагуны (и его вариант вирус Рио Маморе), Андес-подобный вирус Hu39694, Лехигуанаса, Орана, Централ Плата, Буэнос-Айрес, Рио-Мерим, Юквитиба, Юквитиба-подобный, Апе Айме-Итапуа, Араукария, Хабора, Неембуку, Анахатуба, Кастело ду Соньос, Марипо, а также хантавирусы Бермехо в Южной Америке.
Инфекция передается человеку через вдыхание пыли, содержащей частицы выделений американских грызунов семейства хомяковых (особенно оленьей мыши, при передаче вируса Син Номбре). Большинство случаев регистрируются на западе реки Миссисипи весной или летом, как правило, после проливных дождей, что вызывает рост растительности, являющейся источником пищи для грызунов и, таким образом, способствующей росту их популяции.
Симптомы и признаки хантавирусного пульмонального синдрома
Хантавирусный легочный синдром вначале развивается как гриппоподобный синдром с острой лихорадкой, миалгией, головной болью и симптоматикой со стороны желудочно-кишечного тракта. 2–15 дней спустя (в среднем 4 дня) у пациентов быстро появляются признаки некардиогенного легочного отека и гипотония.
У нескольких пациентов были случаи комбинации геморрагической лихорадки с почечным синдромом и легочным синдромом, вызванные хантавирусом. Могут встречаться и легкие формы заболевания.
Диагностика хантавирусного легочного синдрома
Серологический анализ или полимеразная цепная реакция (ПЦР)
Хантавирусный легочный синдром можно заподозрить у пациентов с возможным заражением вирусом, если у них есть необъяснимый клинически или рентгенологически легочный отек. Рентген грудной клетки может показать усиленный сосудистый рисунок, линии Kerley B, двусторонние инфильтраты или плевральные выпоты.
Если данное заболевание заподозрено, то должна быть сделана эхокардио-графия, чтобы исключить кардиогенный легочный отек.
Также обычно выполняют общий анализ крови, анализ на печеночные пробы и анализ мочи. Характерны умеренный нейтрофильный лейкоцитоз, гемоконцентрация и тромбоцитопения. Типично небольшое повышение уровней лактатдегидрогеназы, аспартатаминотрансферазы и аланинаминотрансферазы на фоне уменьшения уровня альбумина в сыворотке. Анализ мочи показывает минимальные отклонения.
Диагноз ГСП ставится по серологическому анализу или обратной транскриптазой-ПЦР.
Прогноз при хантавирусном легочном синдроме
Пациенты с ГСП, которые переживают первые несколько дней, быстро идут на поправку и полностью выздоравливают через 2–3 недели, часто без осложнений. При более тяжелых формах хантавирусного легочного синдрома смертность достигает 50%.
Лечение хантавирусного легочного синдрома
Лечение легочного синдрома, вызванного хантавирусом, поддерживающее. Могут потребоваться механическая вентиляция, тщательный контроль за показателями и сосудосуживающие препараты. При тяжелой сердечно-легочной недостаточности может помочь экстркорпоральная гемооксигенация (см. также Centers for Disease Control and Prevention: Hantavirus Virus: Treatment).

Особенности герпетических инфекций
Герпес — вирусная инфекция, которая характеризуются разнообразием клинических проявлений и может поражать различные системы, органы, ткани:
- нервную систему;
- мочеполовую систему;
- кожный покров и слизистые оболочки;
- глаза.
Для герпетических инфекций характерно пожизненное персистирование — сохранение в организме хозяина. При любом ослаблении иммунной системы происходит реактивация вируса и обострение заболевания. Обострение инфекции могут вызвать разнообразные факторы:
- переутомление;
- переохлаждение;
- стрессы;
- неполноценный сон;
- изменение климатической зоны проживания;
- солнечная инсоляция;
- простудные заболевания.
Выраженность симптоматики зависит от типа и формы течения вируса. При поражении нервной системы заболевание может приводить к воспалению оболочек спинного и головного мозга и другим опасным осложнениям. Поэтому очень важно вовремя диагностировать инфекцию и начать адекватную терапию.
Способы заражения вирусами
Заражение вирусами может происходить воздушно-капельным, контактно-бытовым, половым и гемоконтактным путями. Инфицирование возможно как от больных, так и от носителей вируса. Инфекция достаточно долго сохраняется в высушенном состоянии и может легко передаваться через предметы обихода: чашки, полотенца, игрушки. Также вирус распространяется через слюну, кровь, содержимое везикул, сперму, секрет влагалища и другие среды организма.
Инфекция часто протекает в форме аутоинокуляции, при которой происходит механический перенос вирусных частиц с одного участка на другой. Например, вирус может распространяться по коже и слизистым при расчесах.
Восприимчивость при контакте достаточно высока. Считается, что около 90 % взрослого населения являются носителями того или иного типа герпеса и до 25 % страдают рецидивирующими формами. Как правило, при обследовании часто болеющих детей и взрослых у них обнаруживается несколько вирусов герпеса одновременно.
Виды герпесвирусных инфекций
Известно более 100 представителей вирусов герпетического семейства. Однако наиболее часто человека поражают 8 из них. Рассмотрим подробно особенности и симптоматику самых распространенных инфекций.
Вирус простого герпеса 1 и 2 типа
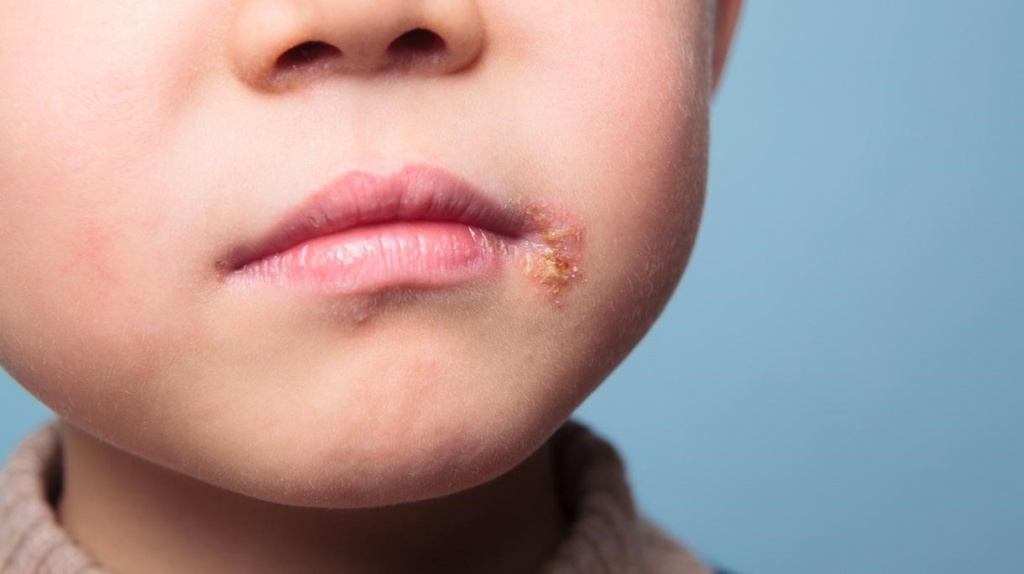
Вирус герпеса первого типа вызывает пузырьковые высыпания на слизистой губ, носа. Как правило, заражение происходит в детском возрасте. К 5-7 годам более 50 % детей являются носителями инфекции. Нередко инфицирование происходит от больных родителей: через поцелуи, предметы обихода.
Инкубационный период длится от 2 дней до 2 недель. Кроме характерных высыпаний, инфекция может сопровождаться повышенной температурой тела, увеличением локальных лимфатических узлов. После поражения слизистых оболочек вирус достигает тройничного нерва, где может оставаться в латентном состоянии длительное время.
Вирус простого герпеса 2 типа или генитальный герпес преимущественно передается половым путем. По России средний показатель составляет 20 % среди взрослого населения. В странах Европы уровень заболеваемости еще выше. В группу риска входят люди, имеющие беспорядочные половые связи. Большая часть заражений происходит во время пубертата, в период начала активной половой жизни.
К симптомам вируса относятся:
- пузырьковые высыпания на половых органах;
- увеличение регионарных лимфоузлов;
- болезненное мочеиспускание;
- зуд в паховой области;
- повышенная температура тела.
Заболевание может протекать с частыми рецидивами (6-12 раз в год и более).
Вирус герпеса 3 типа
Данный вирус может вызывать два заболевания: ветряную оспу и опоясывающий герпес. Как правило, ветряная оспа возникает в детском возрасте и сопровождается характерными признаками:
- везикулярной сыпью, которая сохраняется около 10 дней;
- высокой температурой тела, лихорадкой;
- головной болью;
- зудом кожного покрова;
- симптомами интоксикации организма.
Ветряная оспа у взрослых возникает редко и может протекать в более тяжелой форме: с поражением глаз, нервной системы. В подобной ситуации человеку требуется срочная госпитализация. После заболевания вирус пожизненно сохраняется в организме, находясь в латентном состоянии в нервных узлах.
Вакцинация — самый эффективный способ профилактики заболевания у детей и взрослых, которые в детстве не болели ветряной оспой и не были от нее привиты. Вакцинацию проводят детям с годовалого возраста. Иммунобиологический препарат вводят дважды с интервалом 6 недель. Вакцинацию также проводят в качестве экстренной меры в первые три дня после контакта человека с больным ветряной оспой.
Как правило, опоясывающий герпес встречается у людей старше 65 лет. Заболевание протекает тяжело и сопровождается выраженными симптомами:
- сильными болями;
- нарушением сна;
- высокой температурой;
- высыпаниями везикулярного характера, которые появляются по ходу нервных окончаний.
У заболевания довольно тяжелый реабилитационный период. Даже после исчезновения сыпи у человека долгое время может сохраняться болезненность тех участков, которые были поражены инфекцией. Во всех цивилизованных странах мира проводится вакцинация людей пожилого возраста с целью профилактики опоясывающего герпеса.
Вирус Эпстайна–Барр
Вирус герпеса 4 типа или вирус Эпстайна-Барр поражает человеческий организм комплексно, провоцируя разнообразные и порой никак не связанные между собой патологии. Вирус может вызывать инфекционный мононуклеоз, лимфомы, гепатит, поражать нервную и иммунную системы, кроветворный аппарат.
В человеческой популяции инфицированность вирусом Эпстайна – Барр доходит до 75 % и выше. В группе риска находятся дети старше двух лет и взрослые до 30 лет. Дети до года заболевают редко благодаря пассивному иммунитету, полученному от матери.
Симптоматика заболевания многолика и может иметь различные проявления: от легкого недомогания до выраженных проблем со здоровьем. Самыми распространенными симптомами болезни являются:
- высокая температура, лихорадка;
- боль в горле, мышцах;
- увеличение лимфоузлов, печени, селезенки;
- появление на коже сыпи, шелушений, воспалений, кровоподтеков;
- светобоязнь;
- тошнота.
Характерно, что применение антибиотиков не влияет на длительность лихорадки.
Вирус герпеса 5 типа
Цитомегаловирусная инфекция, вызываемая вирусом герпеса 5 типа, встречается как у детей, так и взрослых. Может протекать по типу мононуклеоза, с высокой температурой, интоксикацией, гнойной ангиной, поражением слюнных желез. Кроме этого, возможно бессимптомное течение инфекции.
Встречаются и врожденные формы заболевания, которые часто приводят к развитию у ребенка тугоухости, микроцефалии, вызывают увеличение печени и селезенки, гематологические расстройства.
Вирусы герпеса 6 и 7 типа
Спектр заболеваний, вызываемых этими вирусами, разнообразен. Часто инфекции протекают в виде внезапной экзантемы. Вирус гепатита 6 типа способен провоцировать синдром хронической усталости, инфекционный мононуклеоз. Считается, что последствием вирусов может стать лимфопролиферативный процесс (образование опухолей лимфатической системы).
Как правило, внезапной экзантемой болеют дети в возрасте до двух лет. Протекает заболевание с высокой температурой, интоксикацией организма. Могут наблюдаться фебрильные судороги, появляется сыпь, которая через несколько дней проходит самостоятельно.
Синдром хронической усталости (СХУ) сопровождается быстрой утомляемостью, снижением работоспособности. Пациентов беспокоит субфебрильная температура, увеличение лимфоузлов, появление катаральных проявлений со стороны глотки.
Вирус герпеса 8 типа
Вирус герпеса 8 типа может вызывать саркому Капоши и болезнь Кастлемана. Саркома Капоши — серьезная патология, которая сопровождается появлением злокачественных новообразований кожи. Протекает достаточно тяжело, особенно при иммунном дефиците. Может осложняться воспалением слизистой неба и лимфоузлов.
Болезнь Кастлемана — редкое заболевание, при котором наблюдаются лихорадочное состояние, увеличение печени, селезенки, анемия, резкое снижение массы тела.
Диагностика герпесвирусных инфекций
Наиболее информативными лабораторными тестами диагностики герпесвирусных инфекций являются ПЦР-метод и иммуноферментный анализ. В зависимости от локализации инфекционного процесса могут исследоваться кровь, слюна, соскобы из уретры, цервикального канала, везикул.
В ходе диагностики определяются качественное и количественное содержание иммуноглобулинов М, G, авидность — показатель, при помощи которого можно оценить насколько продуктивно иммунная система справляется с вирусом.
Для более успешного лечения дополнительно проводится общее обследование организма, позволяющее выявить хронические инфекции. Вялотекущие хронические патологии мочеполовой, дыхательной, пищеварительной и других систем способны поддерживать и вызывать обострение герпесвирусных инфекций.
Особенности лечения герпетических инфекций при беременности
В настоящее время нет точных данных о том, что применение противовирусных средств во время беременности абсолютно безопасно. Поэтому в период гестации, особенно на ранних сроках беременности, не рекомендован прием никаких противовирусных препаратов.
Женщинам, инфицированным герпесом 2 типа, еще при планировании беременности стоит посетить гинеколога и аллерголога-иммунолога для тщательного обследования и лечения. Такие меры позволят снизить число рецидивов во время беременности.
Черная смерть, или чума на протяжении многих столетий считалась неотвратимым приговором. Появление этого грозного заболевания в местности означало лишь одно – смерть практически всего населения, всеобщее горе, запустение и нищету для выживших. За несколько пандемий человеческая цивилизация потеряла сотни миллионов человек, причем чума не щадила ни детей, ни женщин, ни взрослых крепких мужчин.
Историческая справка
Первые достоверные упоминания о болезни, ее симптомах и последствиях относятся к XIV веку. Тогда распространению черной смерти подверглись многие провинции Китая, государства Малой и Средней Азии, Индия. Уже через 10 лет заболевание стало уносить жизни на Ближнем Востоке и на севере Африки. В 1348 году страшная беда пришла на юг Европы, а еще позднее достигла Руси.
Мор от чумы с завидной регулярностью прокатывался по миру, и люди были практически безоружны перед грозным врагом. Вплоть до конца позапрошлого века даже не был выявлен возбудитель заболевания. Обнаружить источник болезни – чумную палочку Yersinia pestis удалось в 1894 году французу А. Йерсену и японцу К. Сибасабуро. Справляться болезнью люди научились позже, и даже в двадцатом столетии чума приносила сметь и страдания на Дальнем Востоке и в Индии. Первые положительные результаты лечения чумы были достигнуты советскими медиками в середине XX века.
Переносчики чумы и пути заражения
Сегодня точно известен не только возбудитель чумы, но и способы распространения болезни. Опасными для человека разносчиками и носителями инфекции являются грызуны, к которым чумная полочка передается через зараженных блох. Медики выделяют несколько географических зон, где риск появления заболевания максимален, но это не значит, что жители других регионов могут пребывать в спокойствии. На сегодняшний день природных очагов инфекции не выявлено только в Австралии.
От блох, в теле которых чумные палочки остаются жизнеспособны до одного года, инфекция попадает в организм крыс и мышей. Они разносят болезнь на огромные расстояния, заражая все новых блох, людей и сородичей. Если учесть, что для паразитирующих на грызунах блох человек является желанной добычей, то риск заболеть в зараженной местности многократно возрастает.
От человека к человеку инфекция передается контактным и воздушно-капельным путем. Опасными могут не только капли мочи, пота или слюны, но и предметы, которыми пользовался больной, а также не подвергнутые обработке продукты питания.
Жизнестойкость возбудителя болезни
Возбудитель чумы отличается высочайшей скоростью размножения и стойкостью к сторонним воздействиям. Палочка не теряет способности размножаться даже при стабильных минусовых температурах, при этом в почве она охраняется до семи месяцев. Притом что без должного лечения смерть человека наступает через 5–10 суток после заражения, на кожных покровах, одежде и предметах, а также в воде Yersinia pestis остается опасной не менее 90 дней.
Смертельной для бактерии оказывается только кипячение, или иное воздействие температурами выше 100 градусов, а также длительное воздействие ультрафиолетового излучения.
Симптомы и формы чумы у человека
От момента проникновения возбудителя в организм до появления первых симптомов проходит от суток до 12 дней. Без принятия срочных мер смертность при чуме составляет 95–100%. Проявляется болезнь остро и ярко, сопровождаясь:
- лихорадкой и ознобом;
- резким подъемом температуры;
- приступами тошноты;
- болезненностью и дискомфортом в суставах.
Кроме присущих многих инфекционным болезням симптомов, у больного:
- на месте проникновения возбудителя появляется покраснении кожи, сыпь, образуются папулы и пустулы;
- в местах расположения лимфатических узлов происходит образование чумного бубона, а сами узлы увеличиваются, воспаляются, отекают;
- наблюдается бледность или посинение кожных покровов, особенно заметное на конечностях и на лице;
- появляется густой белесый налет на языке;
- отмечается скачкообразное изменение давления и пульса;
- снижается свертываемость крови.
При легочной форме у пациента наблюдают кашель с кровью и приступы рвоты, сопровождающиеся кровохарканием.
Современная классификация подразумевает, что заболевание может иметь одну из четырех основных форм: кожной, бубонной, септической и легочной. У всех разновидностей есть свои, не повторяющиеся признаки, однако все виды требуют немедленного принятия мер.
Диагностика и лечение
Практически до середины прошлого века чума не поддавалась лечению, а смертность от нее доходила до 99%. Сегодня ряд бактериологических лабораторных исследований позволяет в кратчайшие сроки, вовремя для начала терапии выявить и нейтрализовать источник опасности. При подозрении на чуму:
- исследованию подлежат места пребывания заболевшего;
- проводятся анализы его мочи, крови, кала, делаются мазки со слизистых;
- делается рентген-диагностика состояния лимфатических узлов.
Сегодня лечение чумы подразумевает борьбу с размножением и патогенным действием возбудителя. Лечение также направлено на облегчение состояния больного и снижению интенсивности симптомов. Неотъемлемая часть терапии – антибиотики.
Читайте также:

